¿Cuál es el nombre del fenómeno que justifica que los metales puedan emitir electrones cuando reciben radiación? Explique cómo se produce dicho fenómeno.
QuímicaMadridPAU 2025Ordinaria
Química · Madrid 2025
7 ejercicios90 min de duración
Ejercicio 1
1
2,5 puntosLa energía solar fotovoltaica es la que se obtiene al convertir la luz solar en electricidad, utilizando una técnica basada en la propiedad que tienen algunos materiales de emitir electrones cuando reciben la radiación solar y aprovechando el movimiento de estos electrones en el material para producir electricidad. Actualmente se usan diversos materiales para construir las celdas solares que forman los paneles solares. En un estudio de los metales Ru y Ce sobre su posible uso para formar parte de paneles solares, se han obtenido los resultados mostrados en la Figura adjunta. Conteste a las siguientes cuestiones:
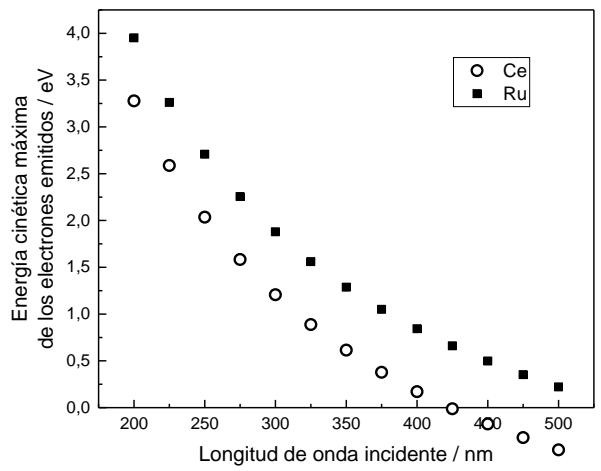
En base a los resultados experimentales representados en la Figura, justifique por qué no se produce electricidad cuando se ilumina la placa de Ce con luz de longitud de onda superior a 425 nm.
Otra de las aplicaciones del Ru es su utilización para formar una aleación con otros metales que se usan en contactos eléctricos para evitar su desgaste. El método consiste en depositar electrolíticamente una capa de Ru sobre el metal a recubrir. Si se dispone de una cuba electrolítica con una disolución acuosa de nitrato de rutenio(II) y se aplica una corriente eléctrica de 1,00 A durante 30 minutos, calcule los gramos de Ru que se depositarán sobre el metal a recubrir.
Ejercicio 2 · Opción A
2Opción A
2,5 puntosElija entre la pregunta 2A y 2B.
Considere las siguientes configuraciones electrónicas:
(A) ;
(B) ;
(C) ; y
(D) .
Conteste razonadamente a las siguientes cuestiones:
¿Alguna corresponde a un estado excitado? En caso afirmativo, razone cuál sería la configuración electrónica del elemento en su estado fundamental.
¿Cuál pertenece a un elemento cuyo anión monovalente tiene estructura de gas noble?
De los elementos (B) o (D), ¿cuál presenta el valor más alto de su primera energía de ionización?
¿Es posible la formación de los compuestos y BD? En caso afirmativo, identifíquelos escribiendo su fórmula e indique el tipo de enlace.
Ejercicio 2 · Opción B
2Opción B
2,5 puntosElija entre la pregunta 2A y 2B.
Considere las sustancias , , , , y .
Indique cuáles presentan enlace covalente y dibuje las estructuras de Lewis de sus moléculas.
De las que no sean covalentes, justifique el tipo de enlace que presentan.
Justifique si son solubles o no en agua cada una de las sustancias del enunciado.
Explique cuál/es conduce/n la corriente eléctrica a temperatura ambiente.
Ejercicio 3 · Opción A
3Opción A
2,5 puntosElija entre la pregunta 3A y 3B.
Complete las siguientes reacciones orgánicas, formulando y nombrando todos los compuestos orgánicos, y especifique de qué tipo de reacción se trata:
A + B etanoato de isopropilo (etanoato de metiletilo)
2-metilpropeno +
butanona + reductor F
Ejercicio 3 · Opción B
3Opción B
2,5 puntosElija entre la pregunta 3A y 3B.
Justifique si las siguientes afirmaciones son verdaderas o falsas, formulando todos los compuestos orgánicos que aparecen:
El pentan-2-ol y el etil propil éter son compuestos isómeros.
El 2-clorobutano presenta isomería cis-trans.
En la siguiente molécula todos los átomos de carbono tienen hibridación :
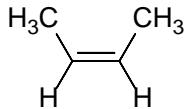
El nombre correcto del compuesto del apartado anterior es trans-but-2-eno.
Ejercicio 4 · Opción A
4Opción A
2,5 puntosElija entre la pregunta 4A y 4B.
Se mezclan 50 mL de una disolución 0,020 M de con 25 mL de una disolución 0,015 M de .
Formule el equilibrio de precipitación del hidróxido de calcio que se produce, detallando el estado de cada especie.
Determine la solubilidad del hidróxido de calcio en y .
Justifique si se forma precipitado de hidróxido de calcio (considere volúmenes aditivos).
Determine el pH de la disolución.
Ejercicio 4 · Opción B
4Opción B
2,5 puntosElija entre la pregunta 4A y 4B.
En un reactor de L se introducen 0,50 mol de y 0,30 mol de a 350 K. Trascurrido un tiempo, se alcanza el equilibrio a una presión total de 3,5 atm. Calcule:
La concentración molar de todas las especies en el equilibrio.
El valor de y .
Justifique cómo afecta al equilibrio un aumento de la presión total del sistema.
