¿Por qué el punto de ebullición del etanol () es aproximadamente mayor que el del dimetiléter () si ambas especies responden a la misma fórmula molecular?
QuímicaMurciaPAU 2016Ordinaria
Química · Murcia 2016
10 ejercicios
Ejercicio 1 · Opción A
1Opción A
2 puntosResponda razonadamente a las siguientes cuestiones:
¿Por qué el ángulo entre los enlaces en el es de aproximadamente , mientras que el ángulo entre los enlaces en el es menor de , si ambas sustancias presentan geometría angular?
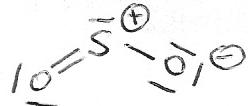

Ejercicio 1 · Opción B
1Opción B
2 puntosConsidere tres elementos (A, B y C) cuyas configuraciones electrónicas en el nivel de mayor energía son: para A; para B y para C.
Indique el grupo de la Tabla Periódica al que pertenece cada uno de ellos.
Indique razonadamente el orden esperado para sus radios atómicos.
Indique razonadamente el orden esperado en sus energías de ionización.
Ejercicio 2 · Opción A
2Opción A
2 puntosCalcule el pH de las siguientes disoluciones acuosas:
, M.
, M.
Datos
Ejercicio 2 · Opción B
2Opción B
2 puntosSi una disolución de ácido benzoico () de concentración está ionizada al , calcule:
La constante de ionización de dicho ácido.
El pH de dicha disolución.
La concentración de ácido benzoico sin ionizar que se halla presente en el equilibrio.
Ejercicio 3 · Opción A
3Opción A
2 puntosFormule o nombre los siguientes compuestos:
peróxido de cobre(I)
fosfato de calcio
cloroformo
ácido pentanodioico
4-metilocta-2,6-diino
Ejercicio 3 · Opción B
3Opción B
2 puntosFormule o nombre los siguientes compuestos:
ácido carbónico
óxido de oro(III)
hidrógenosulfuro de amonio
glicerol
2-etil-5-metilhexanal
Ejercicio 4 · Opción A
4Opción A
2 puntosCalcule a partir de qué temperatura la siguiente reacción será espontánea:
Ejercicio 4 · Opción B
4Opción B
2 puntosEn un recipiente de de capacidad se introducen de a , descomponiéndose de acuerdo con la siguiente reacción:
Sabiendo que en el equilibrio la presión total del recipiente es de , calcule:
El número de moles de cada sustancia en el equilibrio.
El valor de a .
Indique razonadamente cómo evolucionaría el equilibrio al disminuir el volumen del sistema.
Ejercicio 5 · Opción A
5Opción A
2 puntosLa combustión de del compuesto orgánico 2,2,3-trimetilbutano () produjo de medidos a y de presión.
Calcule el rendimiento de la reacción.
Calcule el número de moléculas de contenidas en los del compuesto.
Ejercicio 5 · Opción B
5Opción B
2 puntosAjuste la siguiente reacción de oxidación-reducción usando el método del ion-electrón:
