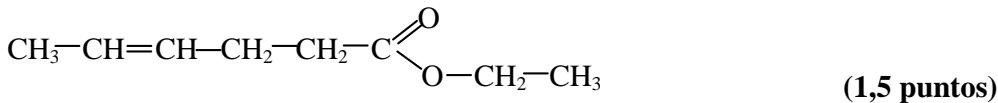Determine la ecuación de velocidad para la reacción, indicando el orden de reacción parcial respecto del reactivo A y del reactivo B.
QuímicaAsturiasPAU 2017Extraordinaria
Química · Asturias 2017
10 ejercicios
Ejercicio 1 · Opción A
1Opción A
2,5 puntosPara la reacción química general , a una temperatura determinada, la velocidad inicial de desaparición de A varía con las concentraciones iniciales de los reactivos en la forma que se indica en la tabla:
| Experimento | [A]0(M) | [B]0(M) | Velocidad inicial (Ms-1) |
| 1 | 0,2 | 0,2 | 2,32 x 10-4 |
| 2 | 0,8 | 0,2 | 9,28 x 10-4 |
| 3 | 1,2 | 1,2 | 8,35 x 10-3 |
Calcule el valor de la constante de velocidad, k, e indique sus unidades.
Ejercicio 1 · Opción B
1Opción B
2,5 puntosEn un recipiente cerrado de , en el que inicialmente se ha realizado el vacío, se introducen moles de , moles de y moles de . La mezcla gaseosa se calienta a , alcanzándose el equilibrio representado por la reacción:
En el equilibrio, la presión parcial de es de .
Indique, de forma razonada, el sentido en el que evolucionará el sistema para alcanzar el equilibrio.
Calcule el valor de para la reacción en equilibrio a , tal y como está escrita.
Ejercicio 2 · Opción A
2Opción A
2,5 puntosCalcule el pH de la disolución resultante de diluir de una disolución acuosa de amoníaco, , al en masa de amoníaco y densidad , con agua hasta un volumen final de la disolución de .
Ejercicio 2 · Opción B
2Opción B
2,5 puntosSe construye una pila voltaica con los siguientes electrodos: a) una tira de cobre sumergida en una disolución acuosa de ; b) una tira de plata sumergida en una disolución acuosa de .
Escriba las semirreacciones de oxidación y de reducción que se producen, de forma espontánea, durante el funcionamiento de la pila. Calcule el potencial estándar de la pila.
Dibuje un esquema de la pila indicando el ánodo, el cátodo y el sentido en el que fluyen los electrones cuando funciona la pila.
Ejercicio 3 · Opción A
3Opción A
1 puntoIndique el material de laboratorio necesario para realizar la determinación de la concentración de en el agua oxigenada comercial, utilizando una disolución de permanganato de potasio.
Ejercicio 3 · Opción B
3Opción B
1 puntoEn la realización de una volumetría ácido-base para determinar la concentración de ácido acético, , en una disolución acuosa, de la disolución acuosa del ácido se diluyen con de agua. La neutralización exacta de esta disolución consume de disolución acuosa de hidróxido de sodio, , .
Calcule la concentración del ácido acético en la disolución inicial.
Indique el nombre del material de laboratorio en el que se alojaría la disolución acuosa de hidróxido de sodio.
Ejercicio 4 · Opción A
4Opción A
2 puntosPara el elemento X, caracterizado por pertenecer al grupo 15 y al período 4 de la tabla periódica: i) escriba la configuración electrónica en el estado fundamental; ii) indique su número atómico; iii) indique el número de electrones desapareados que presenta en el estado fundamental; iv) escriba la configuración electrónica del anión en estado fundamental.
Justifique la diferencia en los valores de las temperaturas normales de ebullición del () y del (), si las dos moléculas presentan la misma estructura molecular (pirámide trigonal) y las dos son polares.
Ejercicio 4 · Opción B
4Opción B
2 puntosIndique el número cuántico, y sus posibles valores, que representa según la teoría mecanocuántica: i) la energía de un orbital; ii) la orientación espacial de un orbital.
Los elementos X e Y ocupan las posiciones de la tabla periódica que se indican a continuación: X periodo = 4, grupo = 13; Y periodo = 4, grupo = 17. Indique el elemento que presentará el valor más alto del radio atómico. Justifique la respuesta.
Ejercicio 5 · Opción A
5Opción A
2 puntosDeduzca el carácter polar, o no polar, de la molécula , que presenta una geometría molecular lineal.
Nombre y escriba las fórmulas semidesarrolladas de los compuestos orgánicos que intervienen en las siguientes reacciones químicas:
Oxidación de 2-propanol (propan-2-ol) con dicromato, , en medio ácido.
Deshidratación del etanol en presencia de ácidos fuertes.
Ejercicio 5 · Opción B
5Opción B
2 puntosIndique el tipo de hibridación del átomo central en las siguientes moléculas: i) (geometría tetraédrica); ii) (geometría lineal).
Identifique y nombre los grupos funcionales presentes en los siguientes compuestos:
Compuesto i
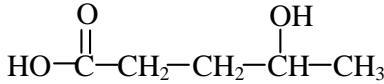
Compuesto ii
Compuesto iii