Número cuántico .
QuímicaLa RiojaPAU 2023Extraordinaria
Química · La Rioja 2023
10 ejercicios
Ejercicio 1
1
2 puntosExplique brevemente el significado de cada uno de los siguientes conceptos:
Apantallamiento.
Energía de red o energía reticular.
Enlace metálico.
Ejercicio 2
2
2 puntosEl carbonato de calcio reacciona con una disolución acuosa de ácido clorhídrico para dar cloruro de calcio, dióxido de carbono (gas) y agua:
Ajuste la reacción química.
Calcule la pureza en carbonato de calcio de una muestra de gramos sabiendo que, al reaccionar completamente con ácido clorhídrico en exceso, se generan gramos de dióxido de carbono asumiendo un rendimiento de reacción del .
Si la reacción de la muestra anterior se lleva a cabo utilizando mL de ácido clorhídrico M, ¿qué cantidad, en gramos, de ácido clorhídrico quedará sin reaccionar?
Ejercicio 3
3
2 puntosLas valoraciones ácido-base son muy útiles para determinar de forma precisa la concentración de ácido o de base en una disolución. Responda a las siguientes cuestiones:
¿Qué es un indicador ácido-base?
¿Qué es el punto de equivalencia de una valoración ácido-base?
Dibuje de forma cualitativa dos curvas de valoración, indicando el pH aproximado del punto de equivalencia (mayor, menor o igual a 7) representando el pH de la disolución respecto al volumen de base fuerte, agente valorante, que se adiciona sobre:
un ácido fuerte.
un ácido débil.
Ejercicio 4
4
2 puntosDos compuestos A y B reaccionan para dar lugar al producto C a de temperatura. Para determinar la cinética de la reacción, se llevaron a cabo los siguientes experimentos:
| Experimento | [A] inicial (mol · L-1) | [B] inicial (mol · L-1) | Velocidad inicial (mol · L-1· s-1) |
| 1 | 0,20 | 0,40 | 64 · 10-3 |
| 2 | 0,20 | 0,20 | 16 · 10-3 |
| 3 | 0,60 | 0,20 | 144 · 10-3 |
Determine el orden de reacción respecto a los reactivos, el orden global de reacción, la ecuación de velocidad y el valor de la constante de velocidad.
Determine la concentración inicial de [B] para que la velocidad de reacción sea si la concentración de [A] es .
Si se añade un catalizador al sistema, ¿cómo afecta a la variación de entalpía entre reactivos y productos () y a la energía de activación del proceso ()?
Ejercicio 5
5
2 puntosRealice un esquema con los principales tipos de isomería estructural en compuestos orgánicos. Añada un ejemplo de cada uno de ellos y nombre correctamente todos los compuestos.
¿Qué compuesto de los siguientes es más soluble en agua? Razone su respuesta.
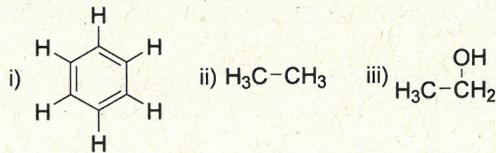
Ejercicio 6
6
2 puntosDetermine la geometría molecular de las siguientes especies químicas utilizando el método que considere oportuno (TEV y/o TRPECV):
Ejercicio 7
7
2 puntosSe preparan mL de una disolución M de un ácido débil HA, cuya constante de ionización es igual a .
Calcule las concentraciones en el equilibrio de , y y el pH de dicha disolución.
¿Cuántos miligramos de hidróxido de sodio sólido son necesarios para neutralizar la disolución del ácido HA?
Si se prepara una disolución a partir de la sal de sodio de la base conjugada (NaA) del ácido HA, ¿la disolución resultante será ácida, básica o neutra? Razone su respuesta.
Ejercicio 8
8
2 puntosEl cobre elemental Cu es un metal relativamente difícil de oxidar. Su reacción con ácidos fuertes como el HCl, no tiene lugar de forma espontánea, mientras que la reacción de HCl con hierro elemental Fe, genera la correspondiente sal de forma espontánea. Razone la veracidad o falsedad de esta afirmación en base a los potenciales de reducción estándar de ambos metales y del par redox .
El ácido nítrico concentrado puede oxidar el cobre metal según la siguiente reacción (no ajustada) en medio ácido. Ajuste la siguiente ecuación mediante el método del ion-electrón en medio ácido y calcule el potencial estándar de la pila voltaica que se podría formar:
Ejercicio 9
9
2 puntosEl hidróxido de magnesio es una sal poco soluble en agua. Sabiendo que su producto de solubilidad es a .
Calcule la solubilidad de dicha sal a en mg/L.
Calcule la solubilidad a en mol/L, del hidróxido de magnesio sólido en una disolución M de nitrato de magnesio.
Ejercicio 10
10
2 puntosNombre los reactivos en negrita, escriba la fórmula semidesarrollada de los productos de las siguientes reacciones orgánicas e identifique el tipo de reacción que tiene lugar en cada caso:
