QuímicaLa RiojaPAU 2015Ordinaria
Química · La Rioja 2015
10 ejercicios90 min de duración
Ejercicio 1 · Opción A
1Opción A
2 puntosFormule o nombre correctamente los siguientes compuestos:
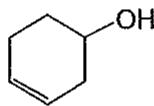
Dimetilcetona
Dihidrogenofosfato de litio
Hidróxido de aluminio
Ejercicio 1 · Opción B
1Opción B
2 puntosExplique razonadamente los siguientes hechos:
El cloruro de sodio tiene un punto de fusión de , mientras que el flúor es un gas a temperatura ambiente.
El etano tiene un punto de ebullición más alto que el metano.
Ejercicio 2 · Opción A
2Opción A
2 puntosEscriba la configuración electrónica de un elemento A de e indique en qué grupo y periodo de la tabla periódica se encuentra.
Indique cuáles son los números cuánticos de cada uno de los electrones que ese elemento posee en su capa de valencia.
Explique razonadamente si el radio de cada uno de los iones y será mayor, menor o igual que el del átomo neutro.
Ejercicio 2 · Opción B
2Opción B
2 puntosIndique razonando su respuesta si las siguientes afirmaciones son ciertas o falsas:
La velocidad de una reacción puede expresarse en .
La constante de velocidad de una reacción de primer orden se expresa en .
Las unidades de la constante de velocidad de una reacción de segundo orden son .
Ejercicio 3 · Opción A
3Opción A
2 puntosDetermine la fórmula empírica de un compuesto gaseoso formado únicamente por boro y flúor sabiendo que en su composición contiene un de boro.
Si de este gas, medidos en condiciones normales de presión y temperatura, ocupan un volumen de , ¿cuál será su fórmula molecular?
Dibuje la estructura de Lewis para esta molécula.
Ejercicio 3 · Opción B
3Opción B
2 puntosA partir de los datos de energía media de enlace de la tabla, determine el valor de la entalpía de hidrogenación del etino a etano:
| enlace | (kJ·mol) |
| C-C | 347 |
| C≡C | 830 |
| C-H | 415 |
| H-H | 436 |
¿Se trata de una reacción endotérmica o exotérmica?
Explique de forma razonada si ese valor de entalpía de reacción será más o menos preciso que el que puede obtenerse a partir de las entalpías de formación de los productos y reactivos.
Ejercicio 4 · Opción A
4Opción A
2 puntosCuando se alcanza el siguiente equilibrio:
a y , la fase gaseosa contiene moles de dióxido de carbono por cada mol de monóxido de carbono.
Calcule las presiones parciales de cada uno de los gases presentes en el equilibrio.
Determine el valor de y del equilibrio a esa temperatura.
Ejercicio 4 · Opción B
4Opción B
2 puntosSabiendo que a la máxima cantidad de sulfato de calcio que puede disolverse en de agua son , determine el valor del producto de solubilidad de dicha sal a esa temperatura. Considere que la densidad de la disolución es .
¿Se formará precipitado al mezclar de disolución de cloruro de calcio con de disolución de sulfato de sodio?
Ejercicio 5 · Opción A
5Opción A
2 puntosPara oxidar zinc a zinc(II) se utiliza una disolución que contiene el ion dicromato en medio ácido, con lo que el dicromato se reduce a cromo(III).
Ajuste por el método ión electrón la reacción de oxidación reducción en su forma iónica e indique qué especie actúa como agente oxidante y cuál como agente reductor.
Calcule el voltaje que se obtendría al formar una pila con un electrodo y un electrodo ambos en condiciones estándar.
Ejercicio 5 · Opción B
5Opción B
2 puntosEl hidróxido potásico contenido en de una muestra de este hidróxido del de pureza, se disuelve en agua para obtener de disolución de hidróxido potásico.
Calcule el pH de la disolución resultante.
Si esta disolución se diluye hasta un volumen de , ¿cuál será el pH de la disolución diluida?
Determine el volumen de ácido clorhídrico necesario para neutralizar de una disolución de hidróxido potásico .
