Escriba y ajuste por el método del ión-electrón, en forma iónica y molecular, la reacción química que tiene lugar, sabiendo que el dicromato se reduce a . Indique la especie que actúa como reductor.
QuímicaAsturiasPAU 2013OrdinariaVariante 1
Química · Asturias 2013
10 ejercicios
Ejercicio 1 · Opción A
1Opción A
2,5 puntosLas entalpías estándar de formación del y del son y , respectivamente. La entalpía estándar de combustión del ácido acético, , es . Calcule la entalpía estándar de formación del ácido acético.
Ejercicio 1 · Opción B
1Opción B
2,5 puntosEn un recipiente de , en el que inicialmente se ha realizado el vacío, se introducen moles de , moles de y mol de . La mezcla se calienta a , alcanzándose el equilibrio:
Si en el equilibrio el número total de moles gaseosos es , calcule los valores de y a .
Ejercicio 2 · Opción A
2Opción A
2,5 puntosUna muestra de gramos de un objeto metálico que contiene un en masa de hierro se trata con diluido hasta que todo el hierro contenido en la muestra se disuelve como . Para oxidar este a , en presencia de , se consumen de una disolución acuosa de dicromato de potasio, , de concentración desconocida:
Calcule la molaridad de la disolución acuosa de dicromato de potasio.
Ejercicio 2 · Opción B
2Opción B
2,5 puntosLa neutralización exacta de de una disolución acuosa de hidróxido de sodio, , necesita de disolución acuosa de ácido clorhídrico, , de . Calcule el de la disolución inicial de .
Ejercicio 3 · Opción A
3Opción A
1 puntoEn un tubo de ensayo se vierten de disolución acuosa de cloruro de sodio, , a la que se añaden gotas de disolución acuosa de nitrato de plata, , hasta la formación de un precipitado claramente visible. Escriba la fórmula química del compuesto que precipita. Se añade a continuación gota a gota disolución acuosa de amoniaco. Indique y explique el cambio que se observa.
Ejercicio 3 · Opción B
3Opción B
1 puntoEn un tubo de ensayo se colocan unos cristales de y se añaden de un disolvente orgánico no polar. Indique y justifique la observación realizada. A continuación se añaden en el mismo tubo de agua, se agita la mezcla y se deja reposar hasta que se separen dos fases. Indique y justifique la coloración que presenta cada una de las fases.
Ejercicio 4 · Opción A
4Opción A
2 puntosEscriba las configuraciones electrónicas de los elementos e e indique el grupo y período de la tabla periódica al que pertenece cada uno de los elementos. A partir de esas configuraciones electrónicas, indique, de forma razonada, el elemento que presenta el valor más bajo del radio atómico.
Deduzca el carácter polar, o no polar, de las siguientes moléculas:
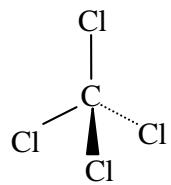
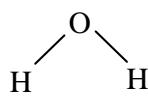
Ejercicio 4 · Opción B
4Opción B
2 puntosIndique, de forma razonada, el número máximo de electrones en un átomo que pueden tener los números cuánticos: y .
Para la reacción: . Indique y justifique si existen condiciones de temperatura en las que la reacción anterior será espontánea.
Ejercicio 5 · Opción A
5Opción A
2 puntosIndique, de forma razonada, el carácter ácido, básico o neutro de una disolución acuosa de .
Datos
Complete la siguiente ecuación química: Indique el tipo de reacción química que tiene lugar, nombre el reactivo, nombre y escriba la fórmula semidesarrollada del producto orgánico de la reacción.
Ejercicio 5 · Opción B
5Opción B
2 puntosIndique, de forma razonada, si la reacción: , transcurrirá de manera espontánea en el sentido en que está escrita. Suponga que reactivos y productos se encuentran en estados estándar.
Datos
Escriba las fórmulas semidesarrolladas de los siguientes compuestos: i) éter metil propílico; ii) 2-propanol; iii) 2-penteno; iv) 1,1,1-clorodifluoroetano.
