Determine el orden de reacción respecto a cada reactivo y el orden total de la reacción. Explique razonadamente las respuestas.
QuímicaCataluñaPAU 2012Ordinaria
Química · Cataluña 2012
7 ejercicios
Ejercicio 1
1
2 puntosUna de las aplicaciones del cloroetano durante el siglo XX ha sido la producción de un antidetonante para la gasolina. El cloroetano se hidroliza en una solución caliente de hidróxido de sodio, según la ecuación siguiente:
Estudiamos la variación de la velocidad inicial de esta reacción para diferentes concentraciones iniciales de los reactivos, a una temperatura determinada. Los resultados se pueden observar en la tabla siguiente:
| Concentración inicial de cloroetano (mol dm⁻³) | Concentración inicial de ion hidróxido (mol dm⁻³) | Velocidad inicial de la reacción (mol dm⁻³ s⁻¹) |
| 0,010 | 0,020 | |
| 0,020 | 0,020 | |
| 0,020 | 0,060 |
Calcule la constante de velocidad de la reacción.
Ejercicio 2
2
2 puntosEn dermatología, el tratamiento de verrugas se lleva a cabo habitualmente de dos maneras diferentes: mediante la criocirugía o congelación de tejidos, o mediante la aplicación de una sustancia corrosiva (procedimiento químico). En este último caso, el principio activo del medicamento empleado es el ácido cloroetanoico (). Este medicamento, que se aplica dos o tres veces al día sobre la verruga, contiene mol de ácido cloroetanoico por cada 100 mL de solución acuosa. Hemos medido el pH de esta solución, a , y hemos obtenido un valor de .
Escriba la reacción del ácido cloroetanoico en agua y explique razonadamente por qué es un ácido, según el modelo de Brönsted-Lowry. Indique cuáles de las especies que intervienen en la reacción, tanto reactivos como productos, actúan de ácido y cuáles de base.
Calcule la constante de acidez del ácido cloroetanoico, a .
Ejercicio 3
3
2 puntosEl proceso de solidificación del agua, a , presenta los valores siguientes:
Suponga que los valores de las variaciones de entalpía y entropía del proceso de solidificación del agua no se modifican con la temperatura, y responda a las cuestiones siguientes:
Explique razonadamente por qué el agua, en condiciones estándar, no se solidifica a , y sí que lo hace a .
Calcule la temperatura, expresada en grados Celsius, por debajo de la cual el agua se solidifica en condiciones estándar.
Ejercicio 4
4
2 puntosEl dióxido de carbono, , es uno de los gases de efecto invernadero más conocidos, ya que absorbe parte de la radiación infrarroja emitida por la superficie de la Tierra. El espectro infrarrojo (IR) del dióxido de carbono muestra que este gas absorbe intensamente la radiación electromagnética de de longitud de onda.
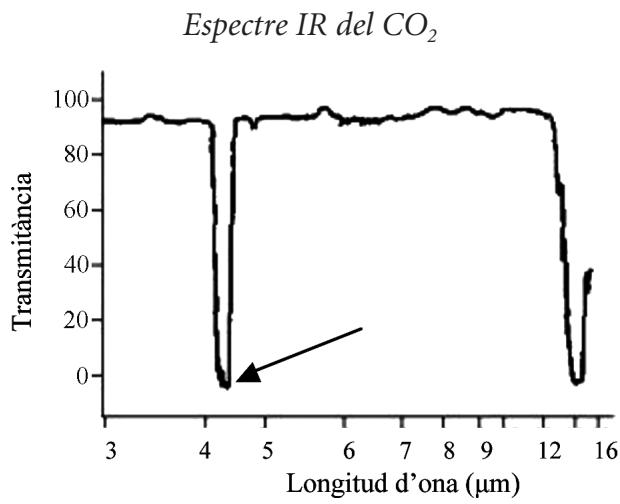
Calcule la frecuencia y la energía de esta radiación absorbida por el dióxido de carbono.
Explique brevemente qué produce la radiación electromagnética infrarroja en una molécula de dióxido de carbono. ¿Por qué las moléculas de este gas absorben solo ciertas longitudes de onda de radiación infrarroja?
Ejercicio 5
5
2 puntosDesarrollamos una sustancia nueva en el laboratorio y comprobamos, experimentalmente, que tiene un punto de fusión a y un punto de ebullición a , a la presión de 1 atm. Mediante experimentos nuevos, encontramos que tiene el punto triple a 0,25 atm y a , y que se sublima a 0,10 atm y a .
Dibuje el diagrama de fases aproximado de esta sustancia e indique en él los puntos de los cuales se conocen datos experimentales.
Explique qué se entiende por punto triple y por punto crítico de una sustancia.
Ejercicio 6
6
2 puntosEn el laboratorio disponemos de las sustancias siguientes:
| Metales | Sn(s) | Cu(s) | Ni(s) |
| Soluciones | KNO₃(aq) 3M | CuSO₄(aq) 1M | NiSO₄(aq) 1M |
¿Qué reacción haría en el laboratorio para conseguir tener una solución acuosa que contuviera iones ? Justifique la respuesta.
Empleando solo las sustancias de la tabla anterior, explique el procedimiento experimental para construir en el laboratorio una pila en condiciones estándar y a , indicando el material necesario. Diga el nombre y la polaridad de cada electrodo.
Ejercicio 7
7
2 puntosEl combustible más utilizado en nuestro país por los automóviles es la gasolina, que está constituida fundamentalmente por octano, . Actualmente se trabaja mucho en una línea de combustibles —denominados biocombustibles— que se obtienen de la materia orgánica originada en un proceso biológico. El bioetanol es un tipo de biocombustible que fundamentalmente contiene etanol, , y que se obtiene de la fermentación de los carbohidratos presentes en la caña de azúcar o el maíz.
| Sustancia | Entalpía estándar de formación, , a 298 K (kJ mol⁻¹) | Entalpía estándar de combustión, , a 298 K (kJ mol⁻¹) |
| -393,5 | ||
| -285,8 | ||
| -5445,3 | ||
| -1369,0 |
Escriba la ecuación de la reacción de combustión del etanol. Calcule la entalpía estándar de formación del etanol a 298 K.
Si la gasolina se vende a 1,30 €/L, ¿cuál deberá ser el precio del etanol, expresado en €/L, para obtener la misma cantidad de energía por euro?
