¿Si la ingesta diaria de los de ácido acetilsalicílico se hace en de agua, se puede asegurar que la concentración ingerida es inferior a ? Razona la respuesta.
QuímicaBalearesPAU 2018Ordinaria
Química · Baleares 2018
10 ejercicios
Datos generales del examen
Ejercicio 1 · Opción A
1Opción A
1 puntoEl ácido acetilsalicílico () es el principio activo de la aspirina, un medicamento que se utiliza como analgésico y antiinflamatorio. En un estudio publicado en 2012 en la revista Lancet se comprobó que un grupo de personas que habían ingerido diariamente y durante cinco años de aspirina reducían en un la incidencia de sufrir un tumor gástrico respecto a las que no ingerían este medicamento.
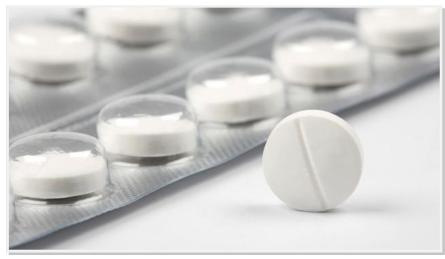
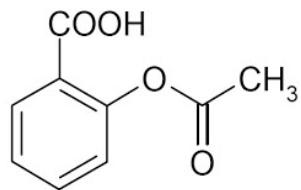
Indica dos grupos funcionales presentes en la molécula de ácido acetilsalicílico (ver la figura 1).
Ejercicio 1 · Opción B
1Opción B
2,5 puntosLa trimetilamina [] es un compuesto orgánico, producto de la descomposición de animales y plantas. Este compuesto es una base débil monobásica.
Calcula el pH de una disolución de trimetilamina que presenta un grado de disociación de .
Calcula la constante de basicidad () de la trimetilamina.
Determina el volumen de una disolución de necesario para neutralizar de la disolución de trimetilamina .
Indica el material de vidrio (su nombre) que utilizarías de los representados en la figura 3 para realizar una valoración ácido-base en el laboratorio de química.




Ejercicio 2 · Opción A
2Opción A
2,5 puntosEl clorato de potasio reacciona con el sulfato de hierro(II) en medio ácido según la reacción ajustada siguiente:
Indica el número de oxidación del cloro en las especies y .
¿Cuál es la especie reductora? ¿Y la especie oxidante? Razona la respuesta.
Determina el volumen de sulfat de hierro(II) necesario para reaccionar con de muestra que contiene un de .
Ejercicio 2 · Opción B
2Opción B
2 puntosLa reacción de isomerización del butano () en metilpropano () viene dada por la reacción ajustada siguiente:
Si inicialmente se inyecta de manera simultánea de butano y de metilpropano en un reactor vacío de que se mantiene a , calcula la concentración de butano cuando se alcanza el equilibrio químico.
Determina la presión parcial de metilpropano cuando se alcanza el equilibrio químico a .
Si se aumenta la presión total del sistema, ¿aumentará la formación de metilpropano? Razona la respuesta.
Ejercicio 3 · Opción A
3Opción A
2 puntosEl presenta el equilibrio químico siguiente:
Indica, razonadamente, si precipitará cuando se mezclan moles de con moles de en de agua.
Sabiendo que el producto de solubilidad () del es , ¿cuál de los dos compuestos es más soluble en agua, el o el ? Razona la respuesta.
Ejercicio 3 · Opción B
3Opción B
2 puntosResponde razonadamente a las preguntas siguientes:
¿Cuál de los tres elementos: , y presenta menor electronegatividad?
Justifica la geometría de la molécula de mediante el modelo de la repulsión de pares de electrones de la capa de valencia. ¿Se puede afirmar que es una molécula apolar?
¿Qué fuerzas de interacción se deben superar para disolver en agua?
Ejercicio 4 · Opción A
4Opción A
2,5 puntosDados los compuestos siguientes: , , y , responde razonadamente a las preguntas siguientes:
¿Qué compuesto es soluble en benceno?
¿Por qué el presenta una temperatura de ebullición superior al ?
¿Qué compuesto conduce la corriente eléctrica en estado fundido? ¿Y en estado sólido?
¿Se puede afirmar que la molécula de presenta un doble enlace?
Ejercicio 4 · Opción B
4Opción B
2 puntosLa notación convencional de la pila Daniell es la siguiente:
Escribe la semirreacción que tiene lugar en el ánodo.
La FEM estándar de la pila Daniell es de . Sabiendo que el potencial estándar de reducción del es de , ¿cuál es el potencial estándar de reducción del ?
Si se cambiase el electrodo de por uno de , ¿aumentaría o disminuiría la FEM de la pila? Razona la respuesta.
Explica qué función tiene un puente salino en una celda galvánica.
Ejercicio 5 · Opción A
5Opción A
2 puntosJustifica si las siguientes afirmaciones son verdaderas o falsas:
Cuando se mezclan de con de , se obtiene una disolución neutra.
El pH de una disolución acuosa de ácido nítrico es menor que el de una disolución de la misma concentración de ácido acético.
La constante de basicidad () del coincide con la constante de acidez () de su ácido conjugado ().
Ejercicio 5 · Opción B
5Opción B
1,5 puntosLa reacción presenta la siguiente ecuación de velocidad: donde a .
Calcula la velocidad de reacción cuando .
En general, ¿se puede afirmar que un aumento de la temperatura disminuye la velocidad de la reacción? Razona la respuesta.
Nombra el compuesto siguiente: .
