Es buena conductora del calor y la electricidad.
QuímicaMurciaPAU 2015Ordinaria
Química · Murcia 2015
10 ejercicios
Ejercicio 1 · Opción A
1Opción A
2 puntosDadas las siguientes sustancias químicas: , , (diamante) y . Indique de forma razonada cuál de ellas:
Presenta moléculas entre las que existen enlaces por puente de hidrógeno.
Presenta el mayor punto de fusión.
Conduce la corriente eléctrica cuando se halla fundida o en disolución acuosa.
Ejercicio 1 · Opción B
1Opción B
2 puntosUn átomo del elemento A presenta la siguiente configuración electrónica: . Justifique razonadamente la veracidad o falsedad de las siguientes afirmaciones:
Dicho átomo se halla en estado fundamental de energía.
El elemento A pertenece al grupo de los halógenos.
es un conjunto de números cuánticos posible para el electrón diferenciador de dicho átomo.
La energía de ionización de A es mayor que la del elemento B, que se encuentra justamente a la derecha de A en la Tabla Periódica.
Ejercicio 2 · Opción A
2Opción A
2 puntosSabiendo que el pH de una disolución acuosa de ácido acético () es igual a ; calcule:
Grado de disociación del ácido en dicha disolución.
Concentración molar del ácido en dicha disolución.
Ejercicio 2 · Opción B
2Opción B
2 puntosJustifique, sin realizar cálculos numéricos, si las siguientes disoluciones son ácidas, básicas o neutras; explicando los procesos que tienen lugar:
Disolución acuosa de cloruro de amonio ().
Disolución acuosa de acetato sódico ().
Ejercicio 3 · Opción A
3Opción A
2 puntosFormule o nombre los siguientes compuestos:
hidróxido de aluminio
hidrogenosulfuro de sodio
butanal
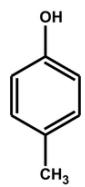
4-metilfenol
ácido oxálico
Ejercicio 3 · Opción B
3Opción B
2 puntosFormule o nombre los siguientes compuestos:
ácido hiponitroso
permanganato de potasio
hidruro de estroncio
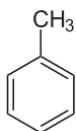
tolueno
4-metil-2-hexino
Ejercicio 4 · Opción A
4Opción A
2 puntosLos calores de combustión bajo condiciones estándar de eteno (), carbono (para producir ) e hidrógeno son , y , respectivamente. A partir de estos datos:
Calcule la entalpía de formación estándar del eteno.
Justifique si la reacción de formación del eteno será espontánea bajo determinadas condiciones de temperatura.
Ejercicio 4 · Opción B
4Opción B
2 puntosEn un recipiente de de capacidad se introducen de y se calienta hasta , descomponiéndose el de acuerdo con la siguiente reacción:
Sabiendo que en el equilibrio la presión total del recipiente es de , calcule .
Indique razonadamente como evolucionaría el equilibrio al aumentar la presión del sistema.
Ejercicio 5 · Opción A
5Opción A
2 puntosConsidere la siguiente reacción química:
Ajústela por el método del ion-electrón.
Calcule el volumen de , medido a y , necesario para que reaccione con de una disolución de de concentración .
Ejercicio 5 · Opción B
5Opción B
2 puntosLa energía de activación correspondiente a la reacción es de , mientras que para la reacción inversa es igual a :
Dibuje de forma detallada un diagrama entálpico que represente la reacción directa.
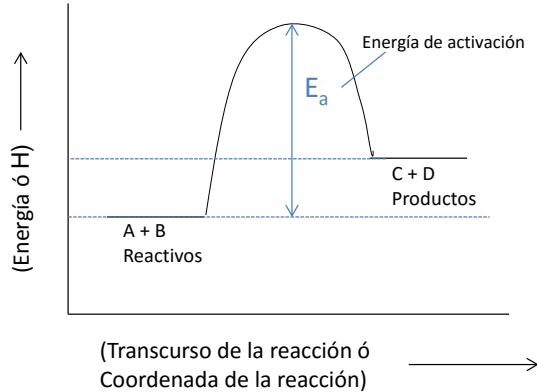
Calcule la variación de entalpía de la reacción inversa, e indique razonadamente si es exotérmica o endotérmica.
Dibuje un diagrama entálpico donde represente el efecto de un catalizador positivo.