Explique brevemente si corresponden a un átomo en estado fundamental, en estado excitado, o si no son posibles.
QuímicaMurciaPAU 2022Extraordinaria
Química · Murcia 2022
10 ejercicios
Ejercicio 1
1
2 puntosConsidere las siguientes configuraciones electrónicas, en las que seis electrones se reparten entre los dos primeros niveles electrónicos:
a)
b)
c)
d)
Considerando que estas configuraciones (las posibles) corresponden a un átomo neutro, indique el nombre y el símbolo atómico del elemento de que se trata.
Si un átomo de dicho elemento pasa de la configuración a) a la c), ¿emitirá o absorberá energía? Justifique brevemente su respuesta.
Explique brevemente cuántos electrones desapareados habrá en la configuración c).
Ejercicio 2
2
2 puntosConsidere las siguientes sustancias: , , , .
Explique de qué dos principales factores depende la energía de red, según la ecuación de Born-Landé y, según ellos, ordene estas sustancias de mayor a menor energía reticular (en valor absoluto).
Explique, de forma general, si las sustancias anteriores conducen la electricidad.
Indique, para las cuatro sustancias en conjunto (sin distinguir entre ellas ni ordenarlas), si sus puntos de fusión serán altos o bajos, si serán solubles en disolventes polares o no polares y si serán sólidos duros o blandos.
Ejercicio 3
3
2 puntosUna reacción transcurre a través de dos etapas elementales:
i)
ii)
Escriba la ecuación global para la reacción.
Si para la reacción global , explique cuál será la etapa de reacción más lenta.
Explique si alguna de las especies involucradas en la reacción es un intermedio.
Explique cómo variarán y durante el transcurso de la reacción.
Ejercicio 4
4
2 puntosEn un tanque cerrado y vacío, de de capacidad, se introducen moles de , moles de y moles de . Para el siguiente equilibrio, a :
¿Está el sistema en equilibrio desde el principio? En caso negativo, ¿hacia dónde se desplazará? Justifique cuantitativamente su respuesta.
Calcule el valor de para el equilibrio anterior a .
Cuando el sistema está en equilibrio, ¿cómo le afectará la apertura de una llave que comunica con otro tanque vacío? Justifique su respuesta.
Ejercicio 5
5
2 puntosSe realiza la valoración de de una disolución de con una disolución de .
Calcule el pH de la disolución inicial de .
¿Qué volumen de la disolución de será necesario para llegar al punto de equivalencia?
Explique qué indicador sería el más adecuado para esta valoración: rojo de cresol (intervalo de viraje: pH ), azul de bromotimol (pH ) o carmín de índigo (pH )?
Calcule el pH de la disolución resultante cuando, desde el inicio de la valoración, se ha añadido un total de de la disolución de (suponiendo que los volúmenes son aditivos).
Ejercicio 6
6
2 puntosConsidere los ácidos y .
Calcule el grado de disociación de una disolución de .
Calcule para la base conjugada del .
En el caso de disoluciones de la misma concentración inicial , explique cuál de los dos ácidos anteriores dará un pH mayor (no es necesario hacer cálculos).
Ejercicio 7
7
2 puntosDada la siguiente reacción redox:
Explique brevemente cuál es el agente oxidante y cuál el reductor.
Ajuste la reacción mediante el método del ion-electrón.
Ejercicio 8
8
2 puntosSe recurre a una celda electrolítica para recubrir una cuchara con una capa de plata. Para ello se sumerge la cuchara en una disolución de y se emplea un electrodo de , actuando la cuchara como el otro electrodo. Conteste a las preguntas:
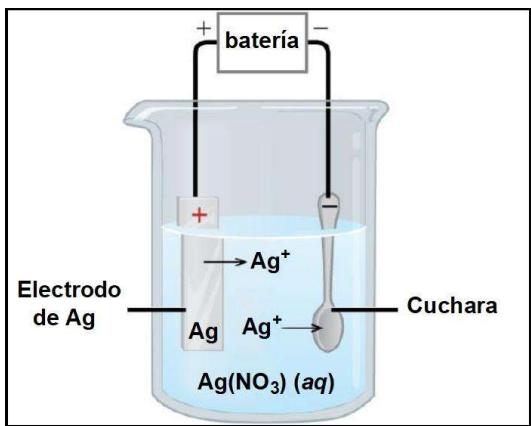
¿La cuchara actúa como ánodo o como cátodo?
Escriba las semirreacciones que tienen lugar en los electrodos, indicando si es una oxidación o reducción.
¿En qué sentido circularán los electrones?
Si se aplica una corriente de durante minutos, ¿qué masa de se depositará en la cuchara?
Ejercicio 9
9
2 puntosCuestiones sobre formulación e isomería orgánica.
Formule o nombre los siguientes compuestos:
a)
b)
c) dietilamina
Indique el tipo y subtipo de isomería que presentan los siguientes pares de compuestos:
a) Los mostrados en las imágenes de estructuras policíclicas.
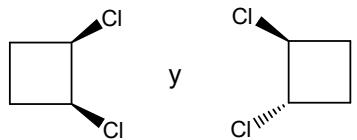
b) Los mostrados en las imágenes de derivados del ciclobutano.
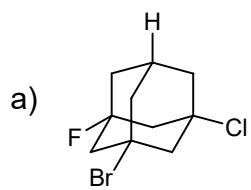
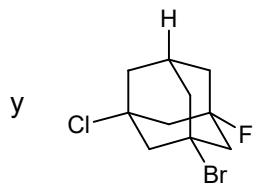
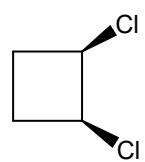
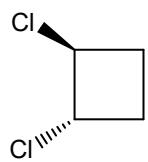
Nombre los dos compuestos del apartado II b) (distinguiéndolos según su isomería).
Indique el tipo de reacción orgánica que ha tenido lugar (una sola palabra es suficiente):
a)
b)
Ejercicio 10
10
2 puntosCuestiones sobre compuestos orgánicos oxigenados y nitrogenados.
Formule los siguientes compuestos:
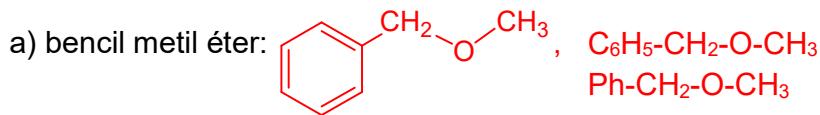
a) bencil metil éter
b) N-etilpropanamida
Dado el compuesto :
Nómbrelo.
Explique si puede presentar algún tipo de isomería espacial (geométrica y/u óptica).
Escriba las fórmulas semidesarrolladas de un isómero estructural de función y otro de posición de dicho compuesto.
Escriba la ecuación química para la reacción de combustión de este compuesto con .
¿Cómo se denomina la siguiente reacción de este compuesto? (una sola palabra es suficiente):
