Dibuje la molécula de amoníaco y justifique sus ángulos de enlace.
QuímicaNavarraPAU 2020Extraordinaria
Química · Navarra 2020
10 ejercicios
Ejercicio 1 · Opción A
1Opción A
2 puntosExplique la hibridación del átomo de nitrógeno en la molécula de amoníaco.
Justifique la polaridad de esta molécula e indique qué fuerzas intermoleculares se darán entre ellas.
Ejercicio 1 · Opción B
1Opción B
2 puntosTenemos dos elementos X e Y. Sus números atómicos son y respectivamente.
Escriba la configuración electrónica de ambos elementos.
Ubíquelos en el Sistema Periódico indicando periodo, grupo, nombre y símbolo de ambos elementos.
Escriba los cuatro números cuánticos del electrón diferenciador del elemento X explicando su decisión.
Justifique los iones que formarán los elementos y qué enlace cabe esperar que se produzca entre ellos, escribiendo la fórmula del compuesto formado.
Ejercicio 2 · Opción A
2Opción A
2 puntosPara la reacción en fase gaseosa: la ecuación de la velocidad es . Indique, justificando su decisión, de qué manera afectan a la velocidad de la reacción las siguientes circunstancias en cada apartado:
La presencia de un catalizador.
Una disminución del volumen del recipiente.
Un aumento de la concentración.
Un aumento de la temperatura.
Ejercicio 2 · Opción B
2Opción B
2 puntosA se introduce cierta cantidad de amoníaco en un recipiente vacío. En esas condiciones, el amoníaco se encuentra disociado en un según el equilibrio siguiente: siendo la presión total del recipiente en el equilibrio . Calcule:
Las presiones parciales de los tres gases en el equilibrio.
Halle y para el citado equilibrio.
Ejercicio 3 · Opción A
3Opción A
2 puntosCalcula la constante de acidez () del ácido débil , sabiendo que una disolución acuosa de este ácido se ioniza al .
Halle el pH de la disolución.
Escriba la reacción entre la base conjugada del ácido y el agua y halle el valor de la constante de ese equilibrio.
Ejercicio 3 · Opción B
3Opción B
2 puntosTenemos una disolución acuosa de ácido hipocloroso de concentración .
Calcule su pH.
Si valoramos de esa disolución de ácido hipocloroso con una disolución de hidróxido de sodio de concentración , calcule el volumen de base que hay que añadir para alcanzar el punto de equivalencia y escriba la reacción.
Razone cualitativamente si, alcanzado el punto de equivalencia, la disolución será ácida, neutra o básica.
Ejercicio 4 · Opción A
4Opción A
2 puntosAjuste por el método del ion-electrón la reacción siguiente: Justifique en la reacción anterior cuál es la especie oxidante y cuál la especie reductora.
Calcule la masa de hipoclorito de sodio que se obtendrá a partir de de cloro.
Ejercicio 4 · Opción B
4Opción B
2 puntosSe realiza la electrólisis del cloruro de cinc fundido.
Indique las reacciones que tienen lugar en el cátodo y ánodo y la polaridad.
¿Cuánto tiempo debe circular una corriente de para conseguir depositar de cinc?
Calcule el volumen de cloro que se desprenderá en ese mismo tiempo, si se mide a una presión de y una temperatura de .
Ejercicio 5 · Opción A
5Opción A
2 puntosFormule los reactivos de las dos reacciones escritas y complételas formulando y nombrando los productos de la reacción:
1) but-1-eno + cloruro de hidrógeno
2) 2-metilbutan-1-ol + ácido sulfúrico concentrado
Clasifique, justificando su decisión, cada una de las reacciones del apartado anterior.
Ejercicio 5 · Opción B
5Opción B
2 puntosNombre el compuesto de la figura. A continuación, formule y nombre tres isómeros de función del compuesto de la figura.
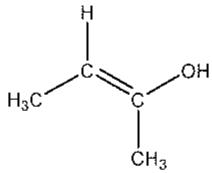
Escriba la reacción de estireno para dar poliestireno, PS.
