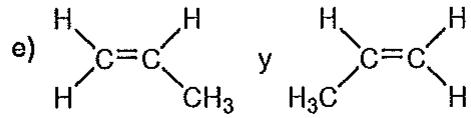Escriba las configuraciones electrónicas de los átomos y y sus iones y .
QuímicaLa RiojaPAU 2017Extraordinaria
Química · La Rioja 2017
10 ejercicios90 min de duración
Ejercicio 1 · Opción A
1Opción A
2,5 puntosRazone sobre la variación de los radios de y al formar los iones y , respectivamente.
Indique los valores que pueden adoptar los números cuánticos , , y para un electrón de número cuántico principal .
¿Qué se entiende por primera energía de ionización de un átomo?
Señale la causa principal por la que la primera energía de ionización del átomo de potasio es menor que la del átomo de cloro.
Ejercicio 1 · Opción B
1Opción B
2 puntosIndique la geometría de las siguientes moléculas haciendo uso de la Teoría de Repulsión de Pares de Electrones de la Capa de Valencia (TRPECV) y razone sobre la polaridad de cada una de ellas:
Ordene las anteriores moléculas en orden creciente de sus ángulos de enlace.
Explique qué tipo de fuerzas intermoleculares contribuyen en mayor medida a mantener en estado líquido las siguientes sustancias:
Ejercicio 2 · Opción A
2Opción A
2 puntosComplete las siguientes reacciones e indique las sustancias que actúan como ácido y como base y sus pares conjugados según la teoría de Brönsted-Lowry:
Ordene razonadamente las siguientes sales en orden creciente del pH que tendrá una disolución de cada una de ellas en agua: cloruro de calcio, acetato de potasio y nitrato de amonio.
Ejercicio 2 · Opción B
2Opción B
2 puntosA y en un recipiente de de capacidad, hay en equilibrio de , de y de .
Calcule las concentraciones de cada una de las especies en el equilibrio.
Calcule el valor de para el equilibrio: a .
Calcule el valor de a esa temperatura.
Indique razonadamente en qué sentido se desplazará el equilibrio si se extrae la mitad del .
Ejercicio 3 · Opción A
3Opción A
2 puntosDetermine el producto de solubilidad () del yoduro de plomo(II) sabiendo que su solubilidad en un litro de agua es .
Calcule la solubilidad del yoduro de plomo(II) expresada en y la concentración de iones yoduro en equilibrio.
Determine si precipitará o no yoduro de plomo(II) al mezclar de una disolución en ion plomo(+2) con de otra disolución en ion yoduro.
Ejercicio 3 · Opción B
3Opción B
2 puntosSe preparan de una disolución disolviendo de ácido acético () en agua. Si esta disolución tiene un :
Determine el valor de la constante de acidez para el ácido acético.
Determine el grado de disociación del ácido acético en la anterior disolución.
Ejercicio 4 · Opción A
4Opción A
2 puntosSe construye una pila con electrodos y , unidos a través de un puente salino que contiene una disolución de cloruro de amonio.
Escriba las semirreacciones que tiene lugar en los electrodos, así como la reacción global, y calcule el valor de la f.e.m. estándar de dicha pila.
Indique cuál será el ánodo y cuál será el cátodo, así como la polaridad de cada electrodo.
Haga una representación gráfica de dicha pila y represente la notación de la misma.
Indique razonadamente en qué sentido se desplazarán los iones amonio y los iones cloruro.
Ejercicio 4 · Opción B
4Opción B
2 puntosLa reacción , de primer orden respecto de A y de segundo orden respecto de B, se lleva a cabo en fase gas en un recipiente de volumen variable.
Formule la expresión de la ecuación de velocidad para esta reacción. ¿Cuál es el orden global de la misma?
Deduzca las unidades de la constante cinética.
Indique razonadamente cómo afectará a la velocidad de reacción un aumento del volumen a temperatura constante.
Indique razonadamente cómo afectará a la velocidad de reacción un aumento de la presión a temperatura constante.
Indique razonadamente cuál es el efecto de un inhibidor o catalizador negativo en la velocidad de reacción.
Ejercicio 5 · Opción A
5Opción A
1,5 puntosPara los compuestos orgánicos de fórmula molecular :
Formule y nombre todos los isómeros posibles.
¿Cuál es la condición necesaria para que un compuesto presente isomería óptica? Indique cuál o cuáles de los anteriores isómeros presentan este tipo de isomería.
Ejercicio 5 · Opción B
5Opción B
1,5 puntosIndique, razonando su respuesta, cuáles de las siguientes parejas de moléculas son isómeros y cuáles no. En caso afirmativo, indique de qué tipo de isomería se trata.
y
y
y
y
Las moléculas representadas en la imagen.