Escriba las configuraciones electrónicas de dichos elementos.
QuímicaLa RiojaPAU 2017Ordinaria
Química · La Rioja 2017
10 ejercicios90 min de duración
Ejercicio 1 · Opción A
1Opción A
2,5 puntosLos elementos que se designan con las letras A, B, C, D y E ocupan las posiciones indicadas en la tabla periódica:
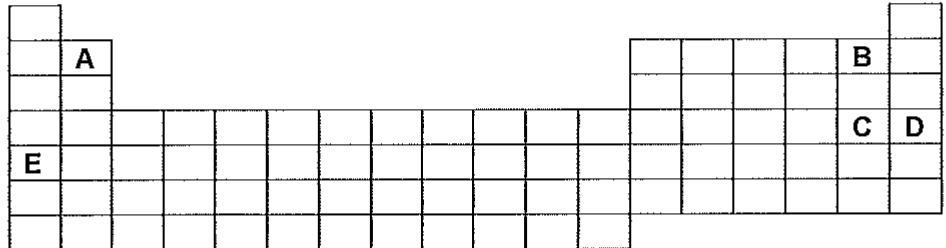
Basándose en ellas justifique de manera razonada si son o no ciertas las siguientes afirmaciones:
La primera energía de ionización de E es mayor que la de A.
D es un gas noble y E un metal alcalinotérreo.
La afinidad electrónica (en valor absoluto) de B es mayor que la de A.
El radio atómico de C es mayor que el de B.
La electronegatividad de C es mayor que la de B.
Ejercicio 1 · Opción B
1Opción B
2,5 puntosExplique qué tipo de enlace químico o qué fuerzas de atracción deben vencerse para llevar a cabo los siguientes procesos:
Fundir bromuro de calcio.
Hervir agua.
Evaporar oxígeno líquido.
Fundir cesio.
Transformar (con enlaces N-O y N-N) en .
Dada la molécula de tetracloruro de carbono:
Represente su estructura de Lewis.
Determine su geometría molecular mediante la Teoría de Repulsión de Pares de Electrones de la Capa de Valencia (TRPECV).
Indique razonadamente cuál es el tipo de hibridación que presenta el átomo de carbono.
Indique si los enlaces en esta molécula son o no son polares.
Indique, razonando su respuesta, si esta molécula es o no es polar.
Ejercicio 2 · Opción A
2Opción A
2 puntosSe dispone en el laboratorio de disoluciones acuosas de concentración de las siguientes sustancias: nitrato de sodio, amoniaco, ácido nítrico, hidróxido de potasio y cloruro de amonio. Ordene razonadamente dichas disoluciones por orden creciente de pH.
Se mezclan de la disolución de ácido acético con de disolución de hidróxido de potasio. Indique, razonando su respuesta y sin necesidad de calcular el valor del pH, si la disolución resultante será ácida, básica o neutra.
Ejercicio 2 · Opción B
2Opción B
2 puntosEn un matraz de de capacidad se introduce una mezcla de de nitrógeno y de oxígeno. Se calienta la mezcla hasta , estableciéndose el equilibrio:
Teniendo en cuenta que en estas condiciones reacciona el del nitrógeno inicial:
Calcule la concentración de todos los compuestos en el equilibrio a .
Calcule el valor de las constantes de equilibrio y a esa temperatura.
¿En qué sentido se desplazará el equilibrio si añadimos una cantidad adicional de nitrógeno? Razone su respuesta.
¿En qué sentido se desplazará el equilibrio si el volumen del matraz disminuye a ? Razone su respuesta.
Ejercicio 3 · Opción A
3Opción A
2 puntosA una disolución saturada de cloruro de plomo(II) tiene una concentración de iones plomo(2+) de .
Calcule cuál es la concentración de iones cloruro en esta disolución.
Calcule a dicha temperatura.
Razone sobre el aumento o disminución de la solubilidad del cloruro de plomo(II) al adicionar cloruro de sodio.
Calcule la solubilidad del cloruro de plomo(II) en una disolución acuosa de concentración en iones plomo(2+).
Ejercicio 3 · Opción B
3Opción B
2 puntosLa reacción es de primer orden respecto de A y de B.
| Experimento | [A]0 mol·L-1 | [B]0 mol·L-1 | velocidad inicial de la reccion |
| 1 | 0,01 | 0,01 | 6·10-4 mol·L-1·s-1 |
| 2 | 0,02 | 0,01 | X1 |
| 3 | 0,01 | X2 | 18·10-4 mol·L-1·s-1 |
A partir de los datos de la tabla, determine el valor de la constante de velocidad, así como de y , indicando sus unidades.
Indique, razonando su respuesta, cuál o cuáles de los términos de la ecuación de velocidad se modificarán al añadir un catalizador y en qué sentido será esa modificación.
Ejercicio 4 · Opción A
4Opción A
2 puntosSe hace reaccionar una muestra de de cobre impuro con una disolución acuosa de ácido sulfúrico, obteniéndose de sulfato de cobre(II), además de dióxido de azufre y agua.
Escriba y ajuste la reacción por el método del ion-electrón.
Calcule la riqueza de la muestra inicial de cobre.
Ejercicio 4 · Opción B
4Opción B
2 puntosSe valoran de una disolución de ácido nítrico con una disolución de hidróxido de potasio .
Calcule el pH de la disolución inicial de ácido nítrico.
Calcule el pH de la disolución tras la adición de de hidróxido de potasio.
¿Cuál será el pH de la disolución en el punto de equivalencia? ¿Cuál de los siguientes sería el indicador más adecuado para esta valoración: azul de timol (viraje: 1-3), rojo de fenol (viraje: 6-8) o amarillo de alizarina-R (viraje: 10-12)?
¿Qué volumen de base será necesario añadir para llegar al punto de equivalencia?
Ejercicio 5 · Opción A
5Opción A
1,5 puntosIndique qué tipo de reacción es cada una de las siguientes:
Ejercicio 5 · Opción B
5Opción B
1,5 puntosFormule o nombre correctamente los siguientes compuestos:
1,3,5-trinitrobenceno
ciclohexeno
