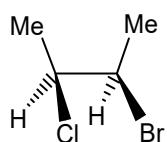
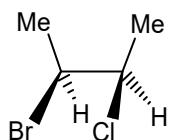
Explique brevemente cuál o cuáles de ellos no son posibles para un electrón en un átomo.
QuímicaMurciaPAU 2021Ordinaria
Química · Murcia 2021
10 ejercicios
Ejercicio 1
1
2 puntosI) Dados los siguientes conjuntos de números cuánticos :
; ; ; ;
II) ¿Qué propiedad periódica describe la tendencia relativa de un átomo para atraer hacia sí los electrones de su enlace con otro átomo? ¿Qué elemento presenta el mayor valor de esta propiedad?
¿Cuál de ellos corresponde a un electrón f?
¿Cuántos electrones puede haber en una subcapa f?
Escriba la configuración electrónica del Fe () y explique si alguno de los conjuntos de números cuánticos anteriores puede corresponder al electrón diferenciador de este elemento.
Ejercicio 2
2
2 puntosI) Considere las siguientes sustancias: , , y .
II) ¿Qué punto de fusión será menor, el del o el del ? Justifique su respuesta.
Indique el tipo de enlace predominante entre los átomos de cada una de ellas.
¿Cuál de ellas presentará mayor conductividad, a temperatura ambiente?
¿En cuál de ellas las moléculas se encontrarán unidas principalmente por enlaces de Van der Waals del tipo dipolo instantáneo - dipolo inducido? Explique en qué consiste este tipo de enlace.
Ejercicio 3
3
2 puntosEl siguiente diagrama entálpico corresponde a la reacción :
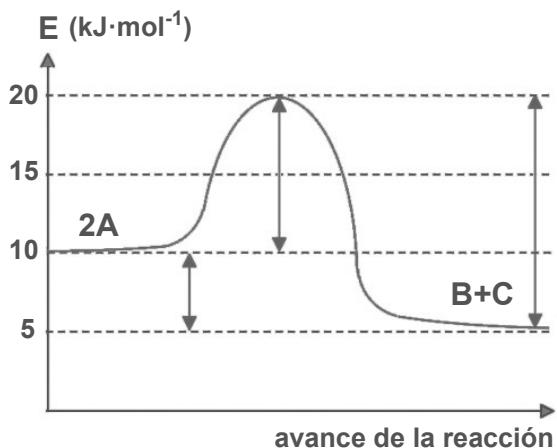
| avance de la reacción | E (kJ·mol⁻¹) |
| 2A | 10 |
| B+C | 5 |
Copie el diagrama en la hoja de respuestas e indique si las flechas corresponden a ( de la reacción directa), (reacción inversa) o .
Fijándose en los valores de , calcule (con su signo correspondiente) , y (reacción directa).
¿Cuál será la energía del estado de transición (complejo activado)?
Escriba la expresión general de (reacción directa) en función de y , y compruebe que se cumple.
Explique si la reacción directa es endotérmica o exotérmica.
Explique si la adición de un catalizador afectaría a la velocidad de la reacción y a .
Ejercicio 4
4
2 puntosSe introduce mol de en un matraz de L que contiene únicamente con una presión de atm, estableciéndose el siguiente equilibrio:
¿Cuál será la presión total () en el matraz cuando se alcance el equilibrio, a ?
¿Cuál será dicha , si inicialmente se introducen moles de , en vez de mol?
¿Cuál es el valor de para el equilibrio anterior, a ?
Ejercicio 5
5
2 puntosI) Calcule el pH de una disolución de que contiene g del ácido por litro de disolución, así como el pH de una disolución de que contiene g de la base por litro de disolución.
II) Calcule el pH resultante si se mezcla L de una disolución de M con L de una disolución de M (suponga que los volúmenes son aditivos).
Ejercicio 6
6
2 puntosSe dispone de disoluciones M de las siguientes sustancias: , , , y . Razone si dichas disoluciones serán ácidas, básicas o neutras, y ordénelas en orden creciente de su pH, justificando su respuesta (no es necesario calcular los valores de pH).
Ejercicio 7
7
2 puntosDada la siguiente reacción de oxidación-reducción:
Explique cuál es el agente oxidante y cuál el reductor. ¿Cuál de ellos cede electrones?
Ajuste la reacción mediante el método del ion-electrón.
Ejercicio 8
8
2 puntosLa electrolisis de una disolución acuosa de origina y .
Escriba las semirreacciones que están teniendo lugar en el ánodo y en el cátodo, indicando si se trata de una oxidación o de una reducción, así como la reacción global del proceso.
Calcule la masa de y el volumen de (medido a y atm) obtenidos al cabo de h de electrolisis, si la corriente aplicada es de A.
Ejercicio 9
9
2 puntosI) Formule o nombre los siguientes compuestos: a) 4-metilhex-2-ino; b) p-bromofenol; c) isobutilamina; d) ; e)
II) Complete las siguientes reacciones orgánicas con todos los productos mayoritarios esperados:
a) Condensación:
b) Adición:
c) Sustitución:
III) Indique el tipo de reacción orgánica que ha tenido lugar (una sola palabra es suficiente):
a)
b)
Ejercicio 10
10
2 puntosI) Formule o nombre los siguientes compuestos: a) 1,2-diclorociclohexano; b)
II) Escriba las fórmulas semidesarrolladas de los siguientes pares de compuestos orgánicos e indique el tipo y subtipo de isomería que presentan entre sí:
a) propanal y acetona
b) pent-1-ino y penta-1,3-dieno
III) Explique si el compuesto puede presentar algún tipo de isomería espacial (geométrica, óptica, ambos tipos o ninguno).
IV) Indique el tipo y subtipo de isomería que presenta el siguiente par de compuestos: