Escriba sus estructuras de Lewis e indique si cumplen no o no la regla del octeto.
QuímicaLa RiojaPAU 2019Extraordinaria
Química · La Rioja 2019
10 ejercicios90 min de duración
Ejercicio 1 · Opción A
1Opción A
2,5 puntosPara las moléculas y :
Determine la geometría molecular utilizando la Teoría de Repulsión de Pares de Electrones de la Capa de Valencia.
Indique, de manera razonada, si se trata de moléculas polares.
Indique, de manera razonada, cuál es la hibridación del átomo central en cada una de estas moléculas.
Ejercicio 1 · Opción B
1Opción B
2,5 puntosDados los elementos de números atómicos , y :
Escriba su configuración electrónica e indique en qué periodo y grupo de la tabla periódica se encuentra cada uno de ellos.
Indique los números cuánticos de todos los electrones del nivel para el elemento .
Indique de manera razonada qué ion es el más estable para cada uno de estos elementos.
Escriba y justifique de manera razonada los elementos del enunciado en orden creciente de su primer potencial de ionización.
Ejercicio 2 · Opción A
2Opción A
2 puntosPara el proceso la constante de equilibrio a vale .
Si se inyecta de en un recipiente de que ya contenía de , calcula las concentraciones de y en el equilibrio a esa temperatura.
Explique razonadamente en qué sentido se desplazará el equilibrio si añadimos una cantidad adicional de .
Explique razonadamente en qué sentido se desplazará el equilibrio si disminuye el volumen del sistema a .
Ejercicio 2 · Opción B
2Opción B
2 puntosSe prepara en el laboratorio una disolución de ácido acético de concentración .
Calcule el grado de disociación del ácido en esta disolución.
Calcule el pH de la disolución.
Calcule el volumen de una disolución de hidróxido de sodio necesario para neutralizar de la disolución de ácido acético.
Justifique de manera razonada si el pH resultante tras la neutralización del apartado anterior será ácido, básico o neutro.
Ejercicio 3 · Opción A
3Opción A
2 puntosLa constante de disociación ácida del ácido hipocloroso, , tiene un valor de . Si se añaden de ácido hipocloroso en la cantidad de agua necesaria para obtener de disolución, calcule:
El grado de disociación.
El pH de la disolución resultante.
Las disoluciones acuosas de cloruro de potasio, bromuro de amonio y acetato de litio presentan en un diferente comportamiento ácido-base. Ordénelas según su valor creciente de pH y justifíquelo de manera razonada.
Ejercicio 3 · Opción B
3Opción B
2 puntosCuando se introduce un fragmento de plata metálica en un recipiente con ácido nítrico se produce una reacción en la que se forman nitrato de plata, monóxido de nitrógeno y agua.
Ajuste las ecuaciones iónica y molecular por el método del ion-electrón.
¿Qué volumen de monóxido de nitrógeno gas, medido a y , se formará por reacción de de plata con ácido nítrico?
¿Qué volumen de disolución de ácido nítrico se necesitaría para que se produzca la reacción del anterior apartado?
Ejercicio 4 · Opción A
4Opción A
2 puntosEl producto de solubilidad, , del fluoruro de calcio es .
¿Cuál es su solubilidad en agua?
¿Cuánto fluoruro de sodio hay que añadir a de una disolución acuosa que contiene de para que empiece a precipitar fluoruro de calcio?
Explique brevemente en qué consiste el efecto del ion común empleando como ejemplo la disolución saturada de fluoruro de calcio.
Ejercicio 4 · Opción B
4Opción B
2 puntosUna reacción química del tipo:
tiene a una temperatura determinada una constante cinética: . Conteste razonadamente a las siguientes preguntas:
¿Cuál es el orden de la reacción anterior?
¿Cómo se modifica el valor de la constante cinética si la reacción tiene lugar a una temperatura inferior?
¿Por qué no coincide el orden de reacción con la estequiometría de la reacción?
¿Qué unidades tendría la constante cinética si la reacción fuera de orden 1?
Ejercicio 5 · Opción A
5Opción A
1,5 puntosFormule o nombre correctamente los siguientes compuestos:
2,2,4-trimetilpentano
fenilmetilcetona
ácido 2,3-dicloropropanoico
Nombre el compuesto de la imagen.
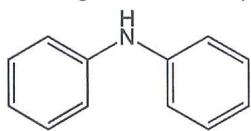
Ejercicio 5 · Opción B
5Opción B
1,5 puntosEscriba las fórmulas de todos los isómeros estructurales de los alquenos de fórmula empírica .
Nombre cada uno de los isómeros anteriores.
Indique cuáles de ellos presentan isomería geométrica y represente y nombre estos isómeros.
Indique cuáles de ellos presentan isomería óptica y señale sus átomos de carbono quirales.
Escriba un ejemplo de adición de con uno de los isómeros del apartado a).
