Escribe y ajusta las semirreacciones de oxidación y reducción utilizando el método del ion-electrón. Indica el nombre del oxidante y del reductor.
QuímicaCastilla-La ManchaPAU 2018Ordinaria
Química · Castilla-La Mancha 2018
10 ejercicios
Ejercicio 1 · Opción A
1Opción A
3 puntosSe puede producir gas cloro haciendo uso de la siguiente reacción:
Ajusta la ecuación molecular.
Calcula los moles de que se producirán si se consumen totalmente de .
Ejercicio 1 · Opción B
1Opción B
3 puntosEl ácido fluorhídrico está disociado al en una disolución cuya concentración es . Calcula:
La constante de disociación del ácido.
El pH de la disolución.
La concentración molar de todos los iones presentes en la disolución.
Ejercicio 2 · Opción A
2Opción A
3 puntosEn un recipiente de litros se introduce una mezcla de de nitrógeno y de hidrógeno. Se eleva la temperatura hasta estableciéndose el equilibrio
En ese instante, se observa que hay moles de amoniaco en la mezcla gaseosa. Calcula:
La constante de concentraciones
La constante de presiones y la presión total de la mezcla gaseosa en equilibrio.
Las presiones parciales de los componentes en el equilibrio.
Ejercicio 2 · Opción B
2Opción B
3 puntosMuchos alcanos, sobre todo los más volátiles, se utilizan como quitamanchas ya que disuelven bien las grasas, aunque son tóxicos e inflamables.
Los cuatro primeros alcanos son gases. Escribe su nombre y su fórmula.
Escribe y ajusta la reacción de combustión de cada uno de ellos.
Dibuja la estructura del primer alcano, explicando el tipo de hibridación del carbono ()
Ejercicio 3 · Opción A
3Opción A
2 puntosLos elementos designados con las letras A, B, C, D y E ocupan las posiciones indicadas en el siguiente esquema de tabla periódica:
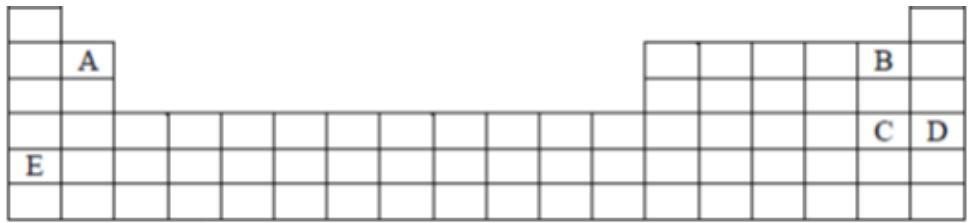
Escribe las configuraciones electrónicas de dichos elementos.
Basándote en ellas justifica si son o no ciertas las siguientes afirmaciones:
La primera energía de ionización de E es mayor que la de A.
D es un gas noble y E un metal alcalinotérreo.
La afinidad electrónica de B es mayor que la de A.
El radio atómico de C es mayor que el de B.
Ejercicio 3 · Opción B
3Opción B
2 puntosJustifica la certeza o falsedad de las siguientes afirmaciones acerca de la velocidad de una reacción:
Se modifica cuando se adiciona un catalizador.
Su valor numérico es constante durante todo el tiempo que dura la reacción.
Su valor numérico aumenta al hacerlo la temperatura a la que se realiza la reacción.
Sus unidades pueden ser
Ejercicio 4 · Opción A
4Opción A
1 puntoEscribe las fórmulas de las bases conjugadas de los siguientes ácidos:
Ejercicio 4 · Opción B
4Opción B
1 puntoEl gas fosgeno, , se obtiene con gran rendimiento mediante el proceso de equilibrio siguiente: Si la concentración de se incrementa mediante la adición de más al sistema en equilibrio, sin cambio de temperatura, ¿cómo se verá afectada:
…la concentración de una vez que se haya alcanzado de nuevo el equilibrio?
…la constante de equilibrio de la reacción?
Ejercicio 5 · Opción A
5Opción A
1 puntoDe los compuestos orgánicos con fórmula molecular , formula y nombra:
Dos isómeros de cadena
Dos isómeros de función.
Ejercicio 5 · Opción B
5Opción B
1 puntoIndica razonadamente si los siguientes procesos de oxidación-reducción pueden tener lugar de forma espontánea:
