¿Es cierto que en el experimento de la figura 1 el cobre oxida la plata?
QuímicaBalearesPAU 2014Ordinaria
Química · Baleares 2014
10 ejercicios
Datos generales del examen
Ejercicio 1 · Opción A
1Opción A
1 puntoDesde el siglo XVI se sabe que cuando se pone en contacto una moneda de cobre con una disolución de nitrato de plata () se forman unos cristales o filamentos que reciben el nombre de árbol de Diana (figura 1) por su semejanza con una especie de vegetación y por su aspecto y color, semejantes a los de la Luna, que antiguamente estaba asociada a la diosa Diana. Responde razonadamente las preguntas siguientes:
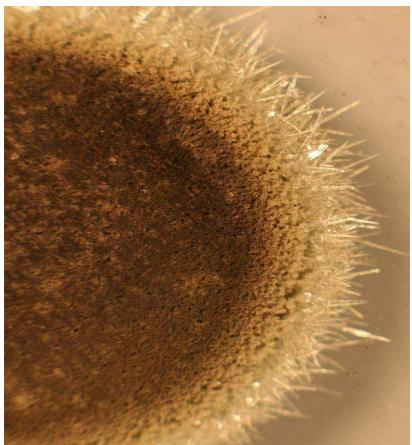
Si la moneda de cobre se pusiera en contacto con una disolución de sulfato de zinc (), ¿se observaría la formación de filamentos?
Ejercicio 1 · Opción B
1Opción B
2,5 puntosEl proceso de fotosíntesis se puede representar por la siguiente ecuación química ajustada:
Calcula la energía necesaria para la formación de de glucosa mediante el proceso de fotosíntesis.
¿Qué volumen de , medido a y , es necesario para la formación de de glucosa mediante el proceso de fotosíntesis?
Calcula la entalpía de formación estándar de la glucosa, .
Ejercicio 2 · Opción A
2Opción A
2,5 puntosUna disolución acuosa de ácido nitroso () tiene un de ácido disociado.
¿Cuál es el pH de la disolución?
Calcula el valor de la constante .
¿Qué volumen de ácido nitroso comercial del en peso en y densidad se necesitaría para preparar de ? Indica el material de vidrio necesario para preparar la disolución.
Ejercicio 2 · Opción B
2Opción B
2 puntosDada la siguiente reacción no ajustada:
Ajusta la reacción iónica por el método del ion-electrón.
¿Cuál es la especie oxidante? Justifica la respuesta.
¿Qué fuerzas se deben romper para disolver en agua?
Ejercicio 3 · Opción A
3Opción A
2,5 puntosEn un recipiente cerrado de dos litros de capacidad y vacío se introduce de . Se mantiene la temperatura a hasta alcanzar el siguiente equilibrio químico:
Calcula la concentración de en el equilibrio.
Calcula el valor de para el equilibrio anterior, a .
Si se aumenta la concentración de , ¿hacia dónde se desplazará el equilibrio químico? Razona la respuesta.
¿Es cierto que si se añade un catalizador, el valor de aumenta?
Ejercicio 3 · Opción B
3Opción B
2 puntosEl ácido fluorhídrico () tiene una constante de acidez, , a . Responde razonadamente si son ciertas o falsas cada una de las afirmaciones siguientes:
El pH de una disolución de es mayor que el pH de una disolución de ácido clorhídrico ().
La constante de basicidad () de la base conjugada del vale a .
Una disolución acuosa de tendrá un pH neutro.
Para neutralizar de una disolución de hacen falta de .
Ejercicio 4 · Opción A
4Opción A
2,5 puntosJustifica la geometría de las moléculas y mediante el modelo de la repulsión de pares de electrones de la capa de valencia.
¿Cuál de las moléculas anteriores es soluble en agua? Razona la respuesta.
¿Qué fuerzas de atracción se deben superar para evaporar ?
Ejercicio 4 · Opción B
4Opción B
1,5 puntosIndica de manera razonada si las siguientes proposiciones son verdaderas o falsas:
Según el principio de Le Châtelier, un aumento de la temperatura favorece que tenga lugar la reacción en el sentido en que sea endotérmica.
Si la constante de equilibrio de una reacción química es mucho mayor que 1, significa que la reacción está muy desplazada hacia los reactivos.
En general, la velocidad de una reacción química es independiente de la concentración de los reactivos.
Ejercicio 5 · Opción A
5Opción A
1,5 puntosPara una cierta reacción química se ha determinado que y .
Indica, razonadamente, si son ciertas o falsas las afirmaciones siguientes:
Se trata de una reacción exotérmica que libera energía.
Es una reacción en la que los productos están más ordenados que los reactivos.
Se trata de una reacción espontánea a cualquier temperatura.
Ejercicio 5 · Opción B
5Opción B
2 puntosUn átomo (X) tiene 35 electrones, 35 protones y 45 neutrones; mientras que otro átomo (Y) tiene 20 electrones, 20 protones y 20 neutrones.
¿Cuál de los dos átomos presenta un mayor radio atómico? Justifica la respuesta.
¿Cuál es el número másico del átomo X?
¿Es cierto que se requiere más energía para arrancar un electrón de X que de Y? Justifica la respuesta.
Indica, razonadamente, si la molécula posee enlaces múltiples o no.
