¿Cómo varía la velocidad de reacción al duplicar la concentración de ? ¿Y si se duplica la concentración de ?
QuímicaNavarraPAU 2021Ordinaria
Química · Navarra 2021
10 ejercicios
Ejercicio 1 · Opción A
1Opción A
2 puntosA la vista de la siguiente tabla periódica, realice la configuración electrónica fundamental de los elementos A, B, C y D. Identifique los elementos y diga cuál sería su estado de oxidación más probable y escriba el ion correspondiente.
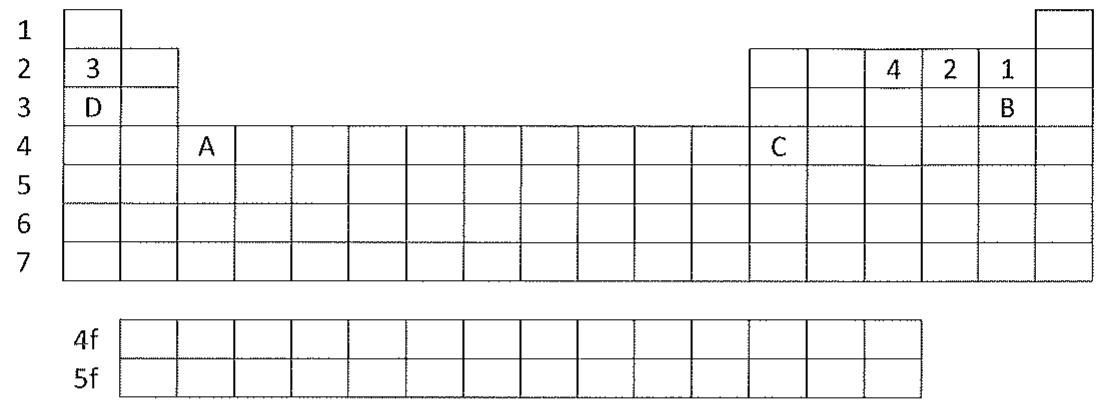
Ejercicio 1 · Opción B
1Opción B
2 puntosRepresente el ciclo de Born-Haber para el óxido de magnesio, , a partir de magnesio y oxígeno en condiciones estándar. Calcule la energía reticular del óxido de magnesio a partir de los siguientes datos:
Ejercicio 2 · Opción A
2Opción A
2 puntosPara la reacción se ha determinado experimentalmente que su ecuación de velocidad es . El mecanismo propuesto es el siguiente:
Etapa 1:
Etapa 2:
Explique brevemente el funcionamiento de un catalizador. ¿Influirá en la velocidad de la reacción? ¿Y en la cantidad de producto obtenido?
Ejercicio 2 · Opción B
2Opción B
2 puntosEn un recipiente de se introducen de , de y de a . Sabiendo que a dicha temperatura es para la reacción :
Indique cómo evolucionará la reacción para alcanzar el equilibrio y las concentraciones de las tres sustancias en el equilibrio.
Calcule el valor de a dicha temperatura.
Ejercicio 3 · Opción A
3Opción A
2 puntosUna disolución de ácido metanoico de concentración tiene el mismo pH que una disolución acuosa de cloruro de hidrógeno de concentración .
Calcule el pH y la constante de acidez del ácido metanoico.
Halle el grado de ionización del ácido metanoico si la concentración inicial de ácido metanoico fuese .
Ejercicio 3 · Opción B
3Opción B
2 puntosTeniendo en cuenta que el cloruro de amonio se disocia completamente en sus iones en disolución acuosa:
Escriba todos los equilibrios que tienen lugar en una disolución acuosa de cloruro de amonio de concentración .
Calcule el pH de dicha disolución.
Ejercicio 4 · Opción A
4Opción A
2 puntosEl estaño reacciona con ácido nítrico y se obtiene óxido de estaño(II), monóxido de nitrógeno y agua.
Escriba la ecuación y ajústela por el método del ion-electrón.
Calcule el volumen de ácido nítrico que se necesitará para convertir todo el estaño que hay en de una aleación ( de estaño en masa) en óxido de estaño(II).
Ejercicio 4 · Opción B
4Opción B
2 puntosUna pila está representada por el siguiente esquema: .
Dibújela señalando cuál es el electrodo positivo y cuál el negativo.
Escriba las dos semirreacciones indicando ánodo y cátodo y qué especie actúa como reductor y cuál como oxidante.
Halle el valor de la fuerza electromotriz de la pila.
Explique qué es un puente salino, ponga un ejemplo de sustancia que pueda actuar como puente salino e indique el movimiento de iones.
Ejercicio 5 · Opción A
5Opción A
2 puntosExplique el concepto de isomería.
Formule y nombre cinco isómeros de un compuesto cuya fórmula corresponde a , señalando el tipo de isomería entre dichos isómeros.
Ejercicio 5 · Opción B
5Opción B
2 puntosFormule los compuestos siguientes: Ácido metanoico, etanonitrilo, etilamina (etanamina), propanamida y propanoato de etilo.
Nombre los siguientes compuestos: , , , , .
Indique si entre las diez sustancias anteriores hay algunas que son isómeros entre sí. En caso afirmativo, identifique el tipo de isomería que presentan.
