2
2 puntosDibuje el ciclo de Born-Haber para la formación del a partir de y , y determine su energía de red, , a partir de los siguientes datos:
Datos
- Entalpía de formación del :
- Entalpía de sublimación del :
- Entalpía de disociación del :
- Energía de ionización del :
- Afinidad electrónica del :
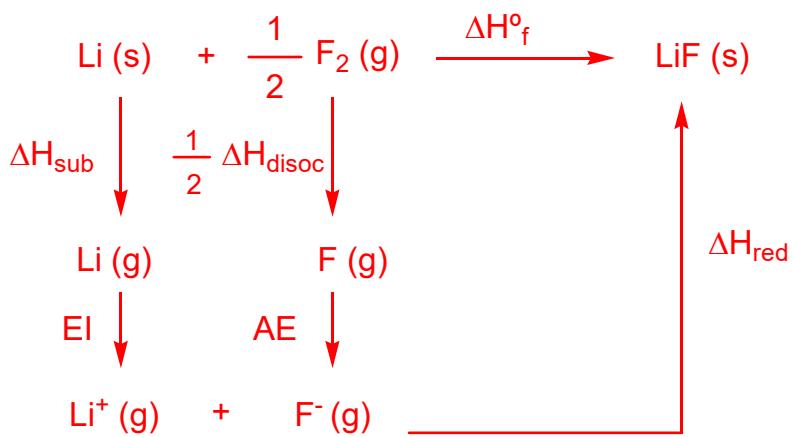
Indique si la energía de red del será mayor o menor (en valor absoluto) que la del . Justifique su respuesta.
