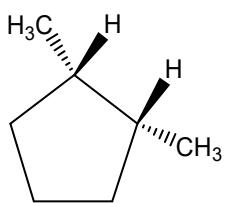
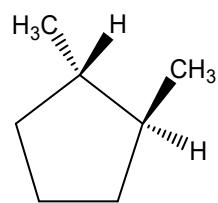
Escriba la configuración electrónica de cada uno de ellos y en base a ella explique cuál será su número de oxidación más importante.
QuímicaMurciaPAU 2020Extraordinaria
Química · Murcia 2020
10 ejercicios
Ejercicio 1
1
2 puntosConsidere los siguientes elementos químicos, consecutivos en la Tabla Periódica: (), (), ().
Al ser consecutivos en la Tabla Periódica, ¿es de esperar que la reactividad de estos tres elementos sea similar? Justifique brevemente su respuesta.
Indique, justificando brevemente su respuesta, cuál de los tres elementos tendrá:
Un mayor radio atómico.
Un mayor potencial de ionización.
Una mayor electronegatividad.
Ejercicio 2
2
2 puntosDibuje el ciclo de Born-Haber para la formación del a partir de y , y determine su energía de red, , a partir de los siguientes datos:
Datos
- Entalpía de formación del :
- Entalpía de sublimación del :
- Entalpía de disociación del :
- Energía de ionización del :
- Afinidad electrónica del :
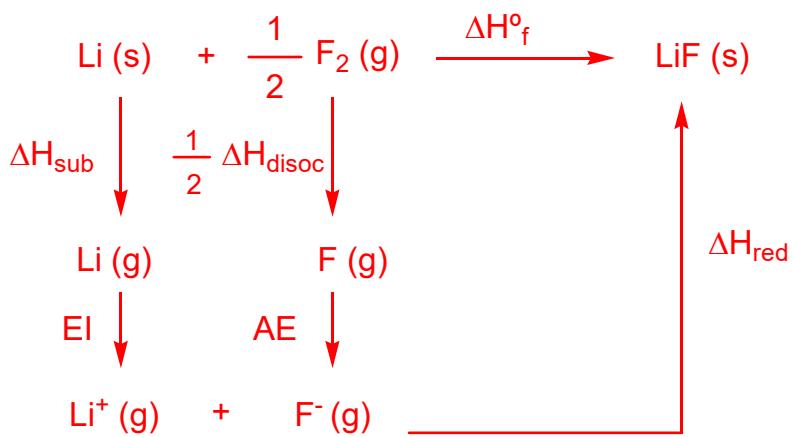
Indique si la energía de red del será mayor o menor (en valor absoluto) que la del . Justifique su respuesta.
Ejercicio 3
3
2 puntosSe sabe que la reacción es de segundo orden con respecto a y de primer orden con respecto a .
Escriba la ecuación de velocidad de la reacción.
¿Es dicha reacción un proceso elemental? Justifique su respuesta.
¿Cuáles son las unidades de la velocidad de reacción () y de la constante de velocidad ()?
¿Cómo variarán la velocidad de reacción () y la constante de velocidad () si se duplica la concentración del reactivo ?
¿Cómo afectará a la velocidad de reacción () y a la constante de velocidad () una disminución de la temperatura?
Ejercicio 4
4
2 puntosEn un recipiente se encuentra una disolución saturada de en agua, en equilibrio con de .
Si la concentración de iones hidroxilo en la disolución es , ¿cuál será la ?
Si se extrae del recipiente del precipitado de , ¿qué ocurrirá con las concentraciones y (aumentarán, disminuirán o permanecerán constantes)? Justifique su respuesta.
Si se adiciona al recipiente una disolución saturada de en agua, de forma que la en la disolución aumenta, ¿qué ocurrirá con el precipitado de (su masa aumentará, disminuirá o permanecerá constante)? Justifique su respuesta.
Calcule la constante del producto de solubilidad () del a si su solubilidad en agua a dicha temperatura es .
Ejercicio 5
5
2 puntosCalcule el volumen de una disolución de necesario para:
Preparar de una disolución de .
Neutralizar de una disolución de .
Ejercicio 6
6
2 puntosSe prepara una disolución de ácido hipocloroso () disolviendo de ácido hipocloroso en de agua. Si , calcule cuál será el grado de disociación del ácido en esa disolución.
Explique si una disolución de hipoclorito sódico () en agua será ácida, básica o neutra. No es necesario realizar cálculos numéricos, pero sí explicar los procesos químicos que tienen lugar.
Ejercicio 7
7
2 puntosDada la siguiente reacción de oxidación-reducción:
Explique cuál es el agente oxidante y cuál el agente reductor.
Ajuste la reacción mediante el método del ion-electrón.
Ejercicio 8
8
2 puntosTeniendo en cuenta los siguientes potenciales estándar de reducción:
Explique qué metal es más reductor: el , el o el . Justifique su respuesta.
Explique si se producirá alguna reacción redox espontánea al adicionar virutas de a una disolución de , en condiciones estándar.
¿Cuál de las siguientes pilas galvánicas será más eficiente, en términos de fuerza electromotriz (diferencia de potencial eléctrico)? Justifique numéricamente su respuesta.
Pila A:
Pila B:
Ejercicio 9
9
2 puntosFormule o nombre los siguientes compuestos:
a)
b)
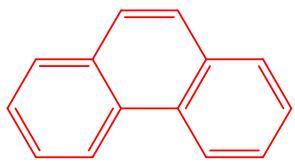
c) fenantreno
d) ácido 4-metilpentanoico
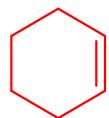
e) ciclohexeno
Complete las siguientes reacciones orgánicas con todos los productos mayoritarios esperados, según el tipo de reacción indicado:
a) Condensación:
b) Eliminación:
c) Combustión:
Indique el tipo de reacción orgánica que ha tenido lugar (una sola palabra es suficiente):
a)
b)
Ejercicio 10
10
2 puntosFormule o nombre los siguientes compuestos:
a) 2-nitropentano
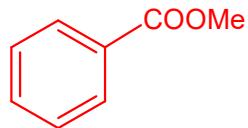
b) benzoato de metilo
Escriba las fórmulas semidesarrolladas de los siguientes pares de compuestos orgánicos e indique justificadamente el tipo y subtipo de isomería que presentan entre sí:
a) 2,4-dimetilhexano y 3-etilhexano.
b) Butanona y but-2-en-2-ol.
Indique justificadamente el tipo y subtipo de isomería que presenta el siguiente par de compuestos orgánicos: