1Opción A
2 puntosEl peróxido de hidrógeno (), llamado también agua oxigenada, se descompone muy lentamente en solución acuosa en oxígeno y agua. La reacción de descomposición se facilita cuando se añaden iones yoduro, y sigue el mecanismo siguiente:
Etapa 1:
Etapa 2:
Cuando estudiamos experimentalmente este mecanismo encontramos que la etapa 1 es la más lenta, y, por tanto, la reacción global sigue una cinética de orden 1 respecto del peróxido de hidrógeno y de orden 1 respecto del ion yoduro.
Escribid la ecuación de velocidad de la reacción de descomposición del peróxido de hidrógeno en presencia de iones yoduro e indicad cuál es el orden total de la reacción. Explicad razonadamente qué función tienen los iones yoduro en este proceso de descomposición y con qué unidades se expresa la constante de velocidad de esta reacción.
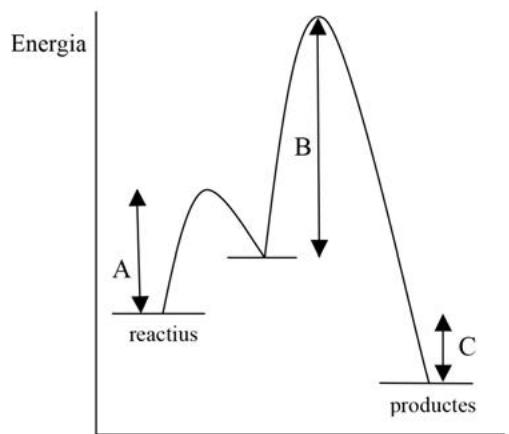
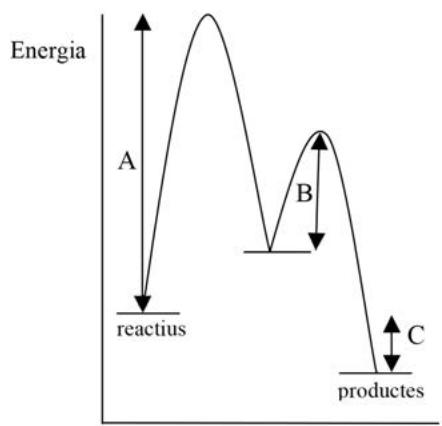
¿Cuál de las dos figuras siguientes representa mejor la descomposición del peróxido de hidrógeno en presencia de iones yoduro y qué magnitudes representan las letras A, B y C? Desde el punto de vista energético, ¿la descomposición es exotérmica o endotérmica? Argumentad las respuestas.