Escribid la ecuación de velocidad de la reacción de descomposición del peróxido de hidrógeno en presencia de iones yoduro e indicad cuál es el orden total de la reacción. Explicad razonadamente qué función tienen los iones yoduro en este proceso de descomposición y con qué unidades se expresa la constante de velocidad de esta reacción.
QuímicaCataluñaPAU 2014Ordinaria
Química · Cataluña 2014
14 ejercicios
Ejercicio 1 · Opción A
1Opción A
2 puntosEl peróxido de hidrógeno (), llamado también agua oxigenada, se descompone muy lentamente en solución acuosa en oxígeno y agua. La reacción de descomposición se facilita cuando se añaden iones yoduro, y sigue el mecanismo siguiente:
Etapa 1:
Etapa 2:
Cuando estudiamos experimentalmente este mecanismo encontramos que la etapa 1 es la más lenta, y, por tanto, la reacción global sigue una cinética de orden 1 respecto del peróxido de hidrógeno y de orden 1 respecto del ion yoduro.
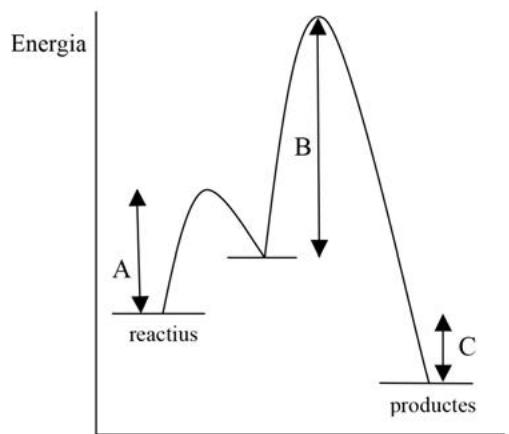
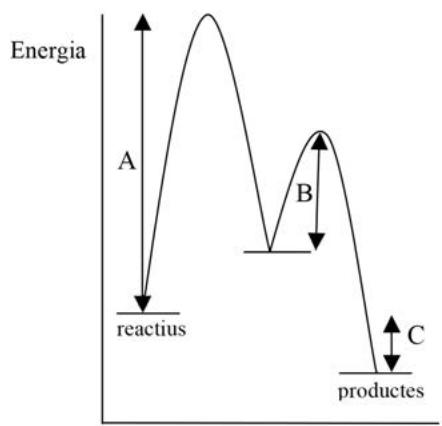
¿Cuál de las dos figuras siguientes representa mejor la descomposición del peróxido de hidrógeno en presencia de iones yoduro y qué magnitudes representan las letras A, B y C? Desde el punto de vista energético, ¿la descomposición es exotérmica o endotérmica? Argumentad las respuestas.
Ejercicio 1 · Opción B
1Opción B
2 puntosEl ácido fluorhídrico es una solución de fluoruro de hidrógeno en agua. Es una sustancia irritante, tóxica y corrosiva. Una de las propiedades del ácido fluorhídrico es que puede atacar el vidrio, y por eso se utiliza para hacer grafías en los llamados vidrios esmerilados. La constante de acidez de este ácido, a , es .
¿Qué pH tiene una solución de ácido fluorhídrico a ?
De los pictogramas de la figura (A-F), indicad los tres que aparecen en la etiqueta de una botella de ácido fluorhídrico. Explicad de qué peligros alertan estos tres pictogramas y decid qué precauciones hay que tomar en la manipulación de ácido fluorhídrico en el laboratorio.

Ejercicio 2 · Opción A
2Opción A
2 puntosLas aguas duras, debido a la presencia de iones calcio y otros iones metálicos, son un problema en los hogares porque pueden formar fácilmente compuestos insolubles como el que provocan averías en las conducciones y en los electrodomésticos.
Una muestra de agua contiene de iones . Calculad la concentración mínima de iones carbonato que debería contener esta agua, en , para que precipite a .
La solubilidad del ¿se mantiene, disminuye o aumenta cuando la sal se disuelve en una solución acuosa de ? ¿Y si se disuelve en una solución acuosa de ácido clorhídrico? Argumentad las respuestas.
Ejercicio 2 · Opción B
2Opción B
2 puntosLas soluciones acuosas de los ácidos reaccionan con muchos metales y producen hidrógeno. Así, por ejemplo, cuando dejamos caer unas cuantas gotas de una solución acuosa de sobre una lámina delgada de aluminio, esta se agujerea debido a la reacción siguiente:
Justificad que esta reacción es espontánea en condiciones estándar y a . Explicad razonadamente qué reactivo es el oxidante y qué reactivo es el reductor.
Podemos llevar a cabo la reacción entre el aluminio y el ácido clorhídrico en una pila para generar corriente eléctrica continua empleando un puente salino de . La notación de esta pila es: Realizad un dibujo de la pila e indicad las polaridades de los electrodos. Justificad hacia dónde se mueven los iones del puente salino cuando la pila está en funcionamiento.
Ejercicio 3 · Opción A
3Opción A
2 puntosEl diamante y el grafito son dos sustancias sólidas formadas solo por átomos de carbono que reciben la denominación de variedades alotrópicas del carbono. La diferencia fundamental en sus propiedades se debe a la disposición espacial de los átomos de carbono.

Calculad la variación de energía libre estándar, , de la transformación química siguiente a , y justificad si es espontánea:
La entalpía estándar de combustión del carbono grafito, a , es . Escribid la reacción de combustión del carbono grafito y calculad la masa mínima que debemos quemar de este compuesto para que el calor liberado se pueda utilizar para calentar de agua contenidos en una olla abierta, a y a presión atmosférica, hasta la temperatura de ebullición. Considerad negligible el calor absorbido por el recipiente.
Ejercicio 3 · Opción B
3Opción B
2 puntosLas energías reticulares de los compuestos iónicos son útiles para predecir los puntos de fusión y las solubilidades en agua de este tipo de compuestos. Para poder calcular el valor de la energía reticular de un compuesto iónico se utiliza el ciclo de Born-Haber. A partir de la figura siguiente:
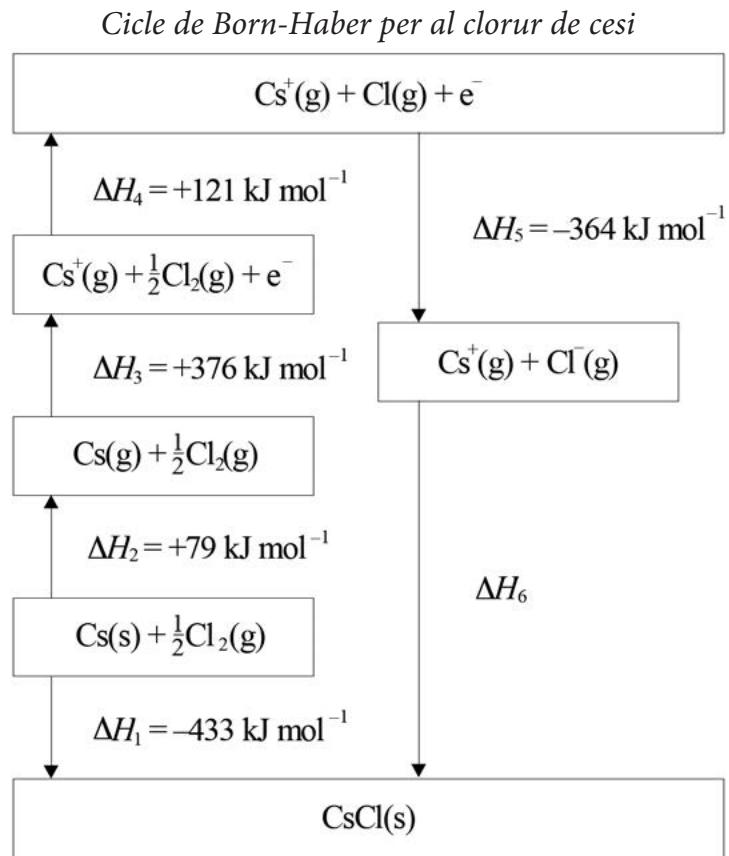
Escribid las reacciones correspondientes a la energía de ionización del cesio, la afinidad electrónica del cloro y la entalpía de formación del cloruro de cesio, e indicad qué valor tienen las entalpías de cada uno de estos procesos.
Calculad el valor de la energía reticular del cloruro de cesio.
Ejercicio 4 · Opción A
4Opción A
2 puntosDada la escasez y el precio tan alto de los derivados del petróleo, se piensa en el hidrógeno como combustible que los puede sustituir, ya que también reacciona con el oxígeno y produce energía en este proceso.

Justificad que se trata de una reacción de oxidación-reducción, e indicad qué reactivo es el oxidante y qué reactivo es el reductor. Explicad razonadamente si la reacción es espontánea, en condiciones estándar y a .
En la naturaleza no hay hidrógeno libre y, por tanto, hay que obtenerlo de alguna manera. El reactivo más barato es el agua y alguien propone utilizar las radiaciones solares para romper directamente el enlace de la molécula de agua, de manera que los radicales formados continuarían la reacción. Justificad si es posible que la radiación solar rompa el enlace , si suponemos que la radiación solar que llega a la superficie terrestre tiene una frecuencia de entre y .
Ejercicio 4 · Opción B
4Opción B
2 puntosEl estaño es un metal plateado, maleable, que no se oxida fácilmente y, por ello, se utiliza en muchas aleaciones para recubrir otros metales y protegerlos de la corrosión. Se puede obtener a partir del óxido de estaño(IV) mediante dos reacciones diferentes:
Reacción A:
Reacción B:
¿Cuál de las dos reacciones tendrá una variación de entropía mayor en condiciones estándar y a ? Explicadlo razonadamente.
Calculad el valor de la energía libre estándar de formación, , del óxido de estaño(IV) a .
Ejercicio 5 · Opción A
5Opción A
2 puntosEl ácido tartárico, , es un ácido orgánico diprótico ya que tiene en la fórmula química dos grupos carboxílicos (). En la industria alimentaria se utiliza como acidificante y conservante natural, y las bebidas refrescantes de frutas lo contienen. En un laboratorio de análisis hemos valorado de una bebida refrescante que contiene ácido tartárico con hidróxido de sodio y hemos necesitado de esta base para que reaccionen los dos grupos carboxílicos.
La recomendación legal es que la concentración de ácido tartárico en las bebidas no supere el valor de . ¿La bebida refrescante analizada está dentro del marco legal?
Detallad el material necesario y el procedimiento experimental para llevar a cabo esta valoración en el laboratorio.
Ejercicio 5 · Opción B
5Opción B
2 puntosLa molécula de -D-glucopiranosa se transforma en su isómero -D-glucopiranosa, en disolución acuosa y a . Este proceso se conoce con el nombre de mutarrotación.
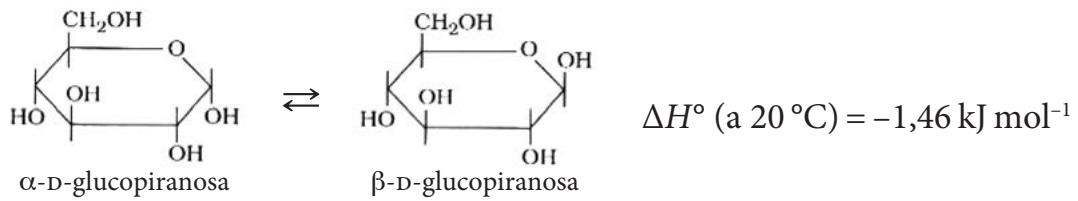
Una solución contiene en equilibrio un en masa de -D-glucopiranosa y un en masa de -D-glucopiranosa, a . ¿Qué valor tiene la constante de equilibrio en concentraciones, , de la reacción de mutarrotación de la -D-glucopiranosa a ?
La mutarrotación de la -D-glucopiranosa a sigue una cinética de primer orden con una constante de velocidad de . Dibujad, de manera aproximada, el perfil de esta reacción en un diagrama de la energía en función de la coordenada de la reacción, suponiendo que la reacción se lleva a cabo en una única etapa, e indicad dónde se encuentra la magnitud de la energía de activación. Cuando la reacción se produce en un medio fuertemente ácido, , la constante de velocidad tiene un valor de . Explicad razonadamente a qué se debe este cambio.
Ejercicio 6 · Opción A
6Opción A
2 puntosEl mecanismo de inflado de un airbag de automóvil se basa en la descomposición de la azida de sodio () que, en menos de , libera una gran cantidad de nitrógeno gaseoso según la reacción en fase heterogénea siguiente:
En un reactor de de capacidad se introducen de azida de sodio y se calienta a para provocar su descomposición. Cuando se alcanza el equilibrio encontramos en el reactor de azida de sodio sin reaccionar.
Determinad la constante de equilibrio en concentraciones, , de la reacción de descomposición de la azida de sodio a .
¿Cómo influirá en la cantidad de azida de sodio descompuesta un aumento de la temperatura si mantenemos constante el volumen del recipiente? ¿Y un aumento del volumen si mantenemos constante la temperatura? Argumentad las respuestas.
Ejercicio 6 · Opción B
6Opción B
2 puntosLas soluciones fertilizantes a base de sulfato de zinc provocan problemas a las plantas cuando se aplican por vía foliar. Para evitar estos efectos tóxicos se recomienda modificar el pH de la solución de sulfato de zinc hasta que empiece a precipitar .

Calculad la solubilidad del , a , expresada en .
Si tenemos una solución fertilizante que contiene de sulfat de zinc, ¿qué pH debemos fijar para que empiece a precipitar ?
Ejercicio 7 · Opción A
7Opción A
2 puntosEn la electrólisis de una solución acuosa de yoduro de potasio () se obtiene y . Para llevar a cabo este proceso de electrólisis en el laboratorio, un estudiante hace el montaje representado en la figura adjunta. El estudiante ha introducido una solución acuosa de yoduro de potasio en el tubo en forma de U, y ha añadido unas gotas de fenolftaleína al lado del tubo donde está el electrodo que hace de cátodo. A medida que avanza el proceso electrolítico, aparecen una coloración rosada en la zona del cátodo y una coloración marronosa en la zona del ánodo.
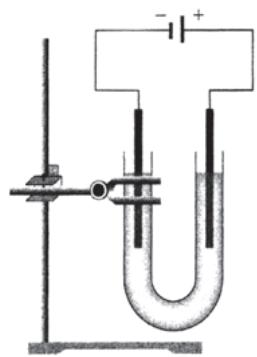
Indicad la polaridad del cátodo y la del ánodo en este proceso electrolítico. Escribid la semirreacción que se produce en el cátodo y explicad razonadamente la coloración que aparece en esta zona.
Escribid la semirreacción que se produce en el ánodo. ¿Qué masa de yodo obtendréis si en el proceso electrolítico circula una corriente de durante ?
Ejercicio 7 · Opción B
7Opción B
2 puntosLa descomposición del ozono en la estratosfera ocurre mediante una cadena de reacciones. La primera consiste en la rotura de una molécula de oxígeno en dos átomos de oxígeno:
Calculad la energía de la radiación electromagnética capaz de producir esta reacción. Explicad razonadamente si la radiación infrarroja podría provocar la rotura de la molécula de oxígeno.
| Frecuencia (Hz) | ||||||
| Radiación | rayos | rayos X | radiación UV-vis. | radiación infrarroja | microondas | ondas de radio |
Definid el término orbital atómico según el modelo ondulatorio del átomo. Escribid la configuración electrónica en estado fundamental del átomo de oxígeno e indicad los números cuánticos del electrón más interno de este átomo.
