1Opción A
1,5 puntosPara las siguientes moléculas: , y
Escriba las estructuras de Lewis y prediga su geometría de acuerdo con el modelo de repulsión de pares electrónicos.
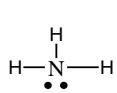
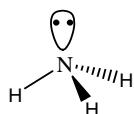
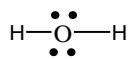
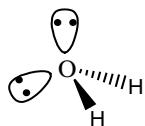
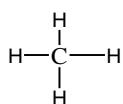
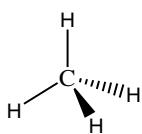
¿Son moléculas polares?
¿Por qué y tienen puntos de ebullición mayores que ?
