5
2,5 puntos# LA QUÍMICA DEL ÁCIDO ACETILSALICÍLICO
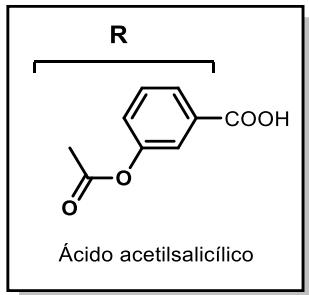
El ácido acetilsalicílico (R-COOH), de masa molar , es el principio activo de la aspirina, uno de los medicamentos más usados en el mundo por sus propiedades analgésicas, antiinflamatorias y antiplaquetarias. Su mecanismo de acción está relacionado con su carácter de ácido débil (), lo que le permite interactuar en diversos procesos biológicos. Sin embargo, esta acidez puede causar irritación gástrica, lo que ha llevado al desarrollo de formulaciones que controlan su liberación en el organismo.
Una tableta típica de aspirina contiene de R-COOH y excipientes que varían según el laboratorio. Algunos de los excipientes que suelen formar parte de su composición incluyen: , utilizado para dar volumen al comprimido; hidróxido de calcio que actúa como regulador del pH; como antiaglomerante; y en formulaciones efervescentes se utiliza el hidrogenocarbonato de sodio que reacciona para liberar dióxido de carbono, lo que causa la efervescencia y ayuda su rápida disolución. Estos excipientes no afectan directamente el equilibrio químico del ácido disuelto, pero aseguran la estabilidad de la tableta y su adecuada disolución en agua.
Se disuelven dos tabletas de aspirina en de agua. Determine el pH de la disolución resultante sin tener en cuenta el efecto de los excipientes.
¿Qué cantidad de ácido acetilsalicílico debe pesarse de un bote de reactivo comercial con una riqueza del para preparar de una disolución ? Indique qué materiales de laboratorio de la siguiente Tabla utilizaría para preparar esta disolución:
| Matraz aforado | Matraz de fondo redondo | Embudo de decantación | Bureta | Vaso de precipitado | Espátula |
Formule o nombre los cuatro excipientes de la aspirina que aparecen en el texto.
