Datos generales del examen
1Opción A
1 puntoEl ha sido ampliamente utilizado por la NASA como comburente de cohetes. Un investigador está interesado en calcular la constante de equilibrio de la reacción de descomposición del a :
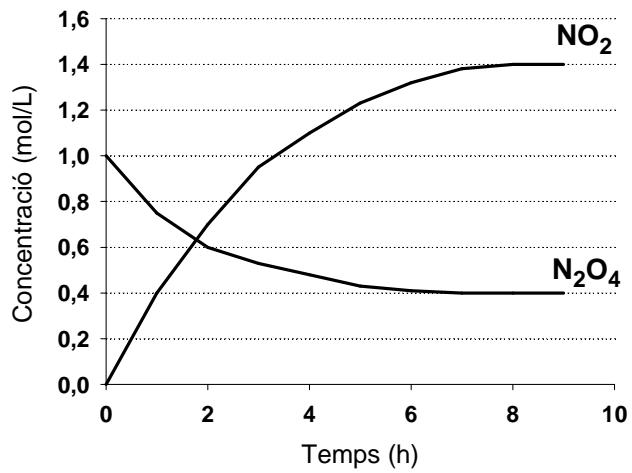
En un experimento, introduce un mol de dentro de un recipiente vacío de un litro de capacidad y determina cómo varían las concentraciones de los compuestos y en función del tiempo (figura 1) a ; mientras que en otro experimento introduce la misma cantidad inicial de y un catalizador específico para esta reacción, y vuelve a determinar la variación temporal de concentraciones (figura 2) a . Justifica la veracidad o falsedad de las afirmaciones siguientes:
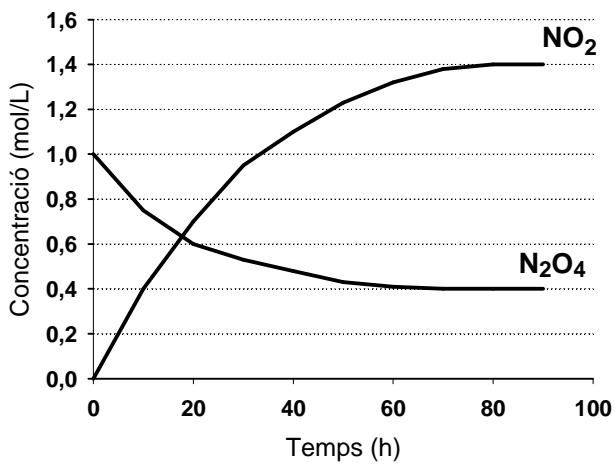
De la figura 1 se puede deducir que a tendrá un valor mucho menor que la unidad.
Cuando se introduce un catalizador en el recipiente que contiene inicialmente el (véase la figura 2), el equilibrio tarda más tiempo en alcanzarse.
