De la figura 1 se puede deducir que a tendrá un valor mucho menor que la unidad.
QuímicaBalearesPAU 2015Ordinaria
Química · Baleares 2015
10 ejercicios
Datos generales del examen
Ejercicio 1 · Opción A
1Opción A
1 puntoEl ha sido ampliamente utilizado por la NASA como comburente de cohetes. Un investigador está interesado en calcular la constante de equilibrio de la reacción de descomposición del a :
En un experimento, introduce un mol de dentro de un recipiente vacío de un litro de capacidad y determina cómo varían las concentraciones de los compuestos y en función del tiempo (figura 1) a ; mientras que en otro experimento introduce la misma cantidad inicial de y un catalizador específico para esta reacción, y vuelve a determinar la variación temporal de concentraciones (figura 2) a . Justifica la veracidad o falsedad de las afirmaciones siguientes:
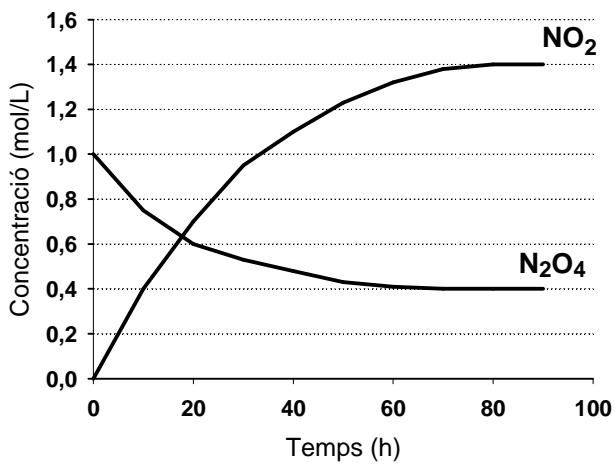
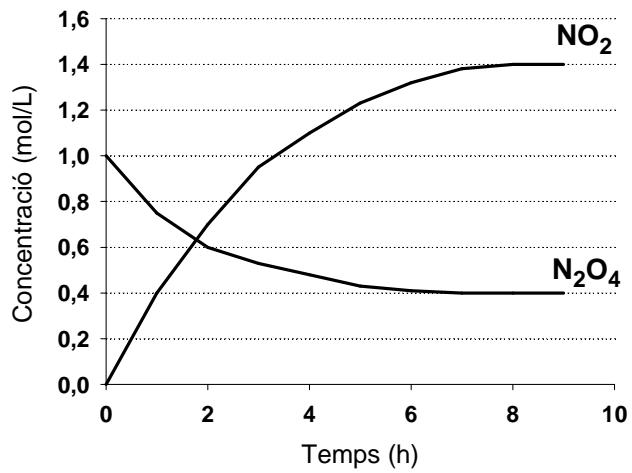
Cuando se introduce un catalizador en el recipiente que contiene inicialmente el (véase la figura 2), el equilibrio tarda más tiempo en alcanzarse.
Ejercicio 1 · Opción B
1Opción B
2 puntosIndica, razonadamente, si son ciertas las siguientes afirmaciones respecto al :
El boro presenta una hibridación en este compuesto.
Se trata de una molécula polar.
La temperatura de ebullición del es mayor que la del .
El primer potencial de ionización del elemento boro es mayor que el del elemento flúor.
Ejercicio 2 · Opción A
2Opción A
2,5 puntosEl estaño metálico reacciona con el según la reacción siguiente:
Escribe y ajusta la reacción iónica y molecular por el método del ion-electrón.
Calcula el volumen de una disolución de ácido nítrico que reaccionará con de estaño.
Nombra las moléculas siguientes: y .
Ejercicio 2 · Opción B
2Opción B
2 puntosEn un laboratorio tenemos una disolución de un ácido monoprótico (AH) con una constante de acidez () de .
¿Es cierto que su grado de disociación es igual a la unidad? Razona la respuesta.
Si se neutraliza la disolución del ácido AH con una base fuerte, como el , ¿es cierto que el pH de la disolución en el punto de equivalencia será menor que ? Razona la respuesta.
Indica el procedimiento y el material de laboratorio para realizar la valoración del apartado b).
Ejercicio 3 · Opción A
3Opción A
2,5 puntosCalcula el pH de una disolución de del en peso y de densidad .
Calcula el pH de la disolución resultante de mezclar de una disolución de con de una disolución de , teniendo en cuenta que los volúmenes son aditivos.
En el recipiente de la disolución de aparece el siguiente pictograma. Indica su significado.

Ejercicio 3 · Opción B
3Opción B
2 puntosEl etano se puede obtener por hidrogenación del eteno en presencia de un catalizador según la siguiente ecuación termoquímica:
Calcula la masa de etano formada a partir de de eteno y de , medidos a y .
Calcula la energía del enlace , si las energías de enlace , y son, respectivamente, , y .
Ejercicio 4 · Opción A
4Opción A
2 puntosConsidera la siguiente reacción química:
Contesta, de manera razonada, las preguntas siguientes:
¿Qué signo tendrá la variación de entalpía de esta reacción?
¿Qué signo tendrá la variación de entropía de esta reacción?
¿Es cierto que esta reacción es espontánea a cualquier temperatura?
¿Por qué motivo el es un gas a temperatura ambiente mientras que el es un líquido?
Ejercicio 4 · Opción B
4Opción B
2 puntosA la constante de equilibrio () de la reacción de descomposición del vale .
En un recipiente cerrado y vacío de se introducen de y de y se mantiene la temperatura a hasta que el sistema alcanza el equilibrio químico.
Calcula la concentración de en el equilibrio.
Determina el valor de para este equilibrio a .
¿Cómo afecta al equilibrio un aumento de la presión total del sistema? Razona la respuesta.
Ejercicio 5 · Opción A
5Opción A
2 puntos¿Cuál de los siguientes elementos tiene menor radio atómico: oxígeno o fósforo? Razona la respuesta.
Indica, razonadamente, el número de electrones desapareados que tiene el fósforo en su estado fundamental.
Para la molécula de eteno , deduce la estructura de Lewis e indica, de manera razonada, el tipo de hibridación de los átomos de carbono.
Ejercicio 5 · Opción B
5Opción B
2 puntosDados los siguientes metales: cobre y níquel. Contesta razonadamente las cuestiones siguientes, considerando condiciones estándar en todos los casos:
Ordena los metales de mayor a menor poder reductor.
¿De estos metales, alguno podrá reducir el ion a ?
Determina la fem estándar de la pila formada por los electrodos de y que funciona espontáneamente.
¿Qué utilidad tiene un puente salino en una pila galvánica?
