4Opción B
2 puntosConsidere la siguiente reacción química reversible: , cuyas energías de activación para la reacción directa () e inversa () son: ; .
Represente la reacción en un diagrama de energía frente a avance de la reacción (diagrama entálpico o perfil de reacción), indicando la situación de reactivos, productos y complejo activado (estado de transición), las energías de activación (, ) y la variación de entalpía de reacción ().
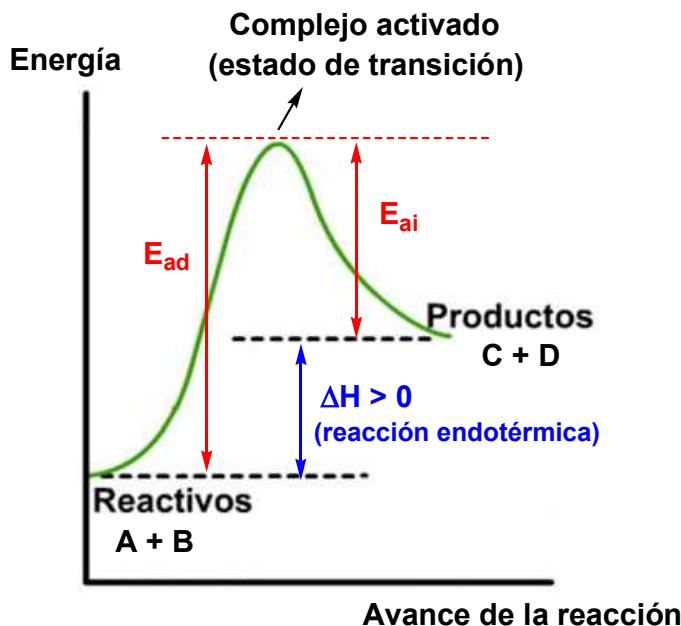
Calcule y diga si la reacción es endotérmica o exotérmica.
¿Qué efecto tendría la adición de un catalizador eficiente (un catalizador positivo), en la y en la ?
