Indique su nombre y símbolo atómico, y el grupo y periodo en que se encuentran.
QuímicaMurciaPAU 2019Extraordinaria
Química · Murcia 2019
10 ejercicios
Ejercicio 1 · Opción A
1Opción A
2 puntosDados los elementos A, B y C, con las siguientes configuraciones electrónicas:
A:
B:
C:
Explique brevemente cuál de ellos tendrá:
Mayor afinidad electrónica.
Mayor carácter metálico.
Tendencia a perder o ganar tres electrones.
Menor radio atómico.
Ejercicio 1 · Opción B
1Opción B
2 puntosPara cada una de las siguientes moléculas: , y
Represente su estructura de Lewis.
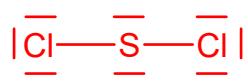
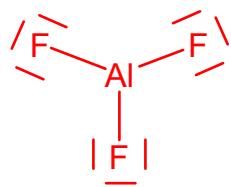
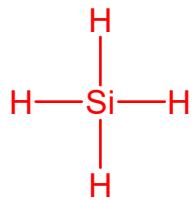
Justifique su geometría según la teoría de repulsión de pares de electrones en la capa de valencia.
Explique si son polares o apolares.
Ejercicio 2 · Opción A
2Opción A
2 puntosCalcule el pH de las siguientes disoluciones:
Disolución acuosa de M.
Disolución formada al mezclar mL de una disolución de M y mL de una disolución de M. Considere los volúmenes aditivos.
Ejercicio 2 · Opción B
2Opción B
2 puntosUna disolución acuosa de M tiene un pH igual a . Calcule para dicho ácido:
Su grado de disociación.
Su constante de acidez.
Ejercicio 3 · Opción A
3Opción A
2 puntosFormule o nombre los siguientes compuestos:
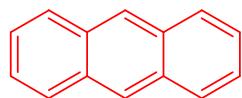
a) Antraceno
b) Ciclohexino
c) Etil fenil éter
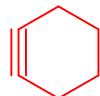
d)
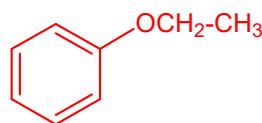
e)
Indique el tipo de reacción orgánica que ha tenido lugar:
a)
b)
c)
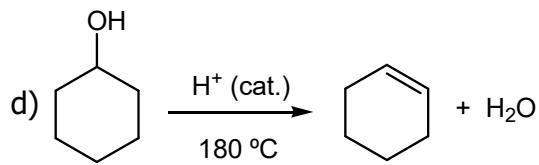
d) Reacción mostrada en la imagen correspondiente.
Ejercicio 3 · Opción B
3Opción B
2 puntosFormule o nombre los siguientes compuestos:
a) Ciclooctano
b)
c) Pentano-2,4-diona
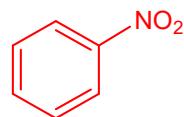
d)
e) Nitrobenceno

Explique el tipo de isomería que presentan los siguientes pares de compuestos:
a) y
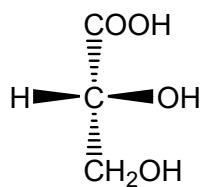
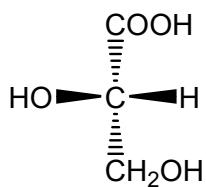
b) Enantiómeros del ácido láctico (ver imagen).
c) Isómeros del 1,2-diclorociclohexano (ver imagen).
d) y

Ejercicio 4 · Opción A
4Opción A
2 puntosEn un recipiente cerrado de mL en el que se ha hecho vacío, se introducen g de y g de y se calienta hasta , alcanzándose el siguiente equilibrio:
Calcule la presión total en el equilibrio.
Si en el equilibrio hay moles de , calcule la concentración molar de cada una de las especies en el equilibrio y los valores de y a .
Ejercicio 4 · Opción B
4Opción B
2 puntosConsidere la siguiente reacción química reversible: , cuyas energías de activación para la reacción directa () e inversa () son: ; .
Represente la reacción en un diagrama de energía frente a avance de la reacción (diagrama entálpico o perfil de reacción), indicando la situación de reactivos, productos y complejo activado (estado de transición), las energías de activación (, ) y la variación de entalpía de reacción ().
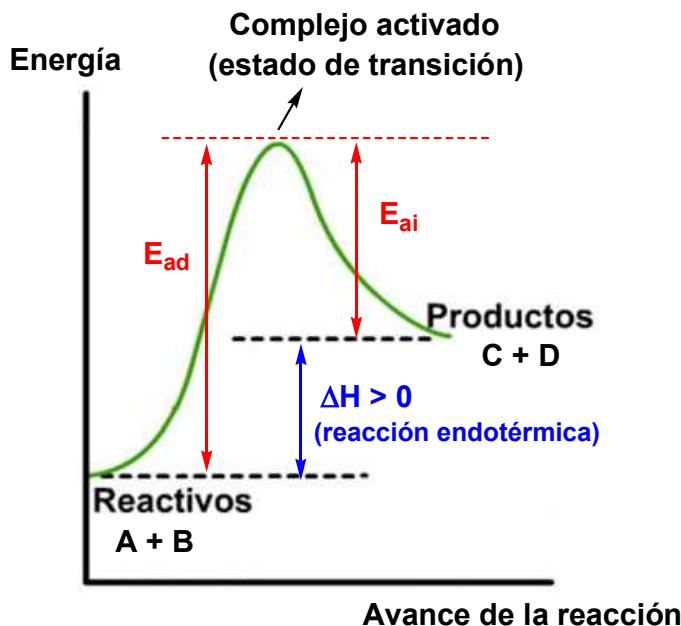
Calcule y diga si la reacción es endotérmica o exotérmica.
¿Qué efecto tendría la adición de un catalizador eficiente (un catalizador positivo), en la y en la ?
Ejercicio 5 · Opción A
5Opción A
2 puntosDada la reacción de oxidación-reducción:
Explique cuál es el agente oxidante y cuál el agente reductor.
Ajuste la reacción mediante el método del ion-electrón.
Ejercicio 5 · Opción B
5Opción B
2 puntosSe dispone de la siguiente pila galvánica:
Escriba las reacciones que tienen lugar en cada uno de los electrodos, identificándolos como cátodo o ánodo, así como la reacción global de la pila.
Calcule la fuerza electromotriz de la pila.
Calcule la variación de energía libre.
