2
2,5 puntosLa determinación de propiedades atómicas y la modelización de las estructuras formadas por interacción entre átomos han sido esenciales en la construcción del conocimiento de la química. El desarrollo de nuevas sustancias y materiales y el análisis estructural continúan siendo focos de atención en proyectos de investigación e innovación.
El enlace covalente y el enlace iónico son modelos muy útiles para interpretar las propiedades de las sustancias, pero los enlaces reales tienen un porcentaje de enlace covalente e iónico que se basa sobre todo en la diferencia de electronegatividad. En general, si la diferencia de electronegatividad entre los átomos es superior a , el enlace tendrá más de un de carácter iónico, mientras que si es inferior a , el porcentaje de carácter iónico será de menos del .
| Átomo | Número atómico (Z) | Electronegatividad |
| H | 1 | 2,1 |
| Li | 3 | 1,0 |
| Be | 4 | 1,5 |
| O | 8 | 3,5 |
| Cl | 17 | 3,0 |
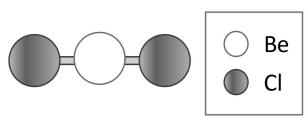
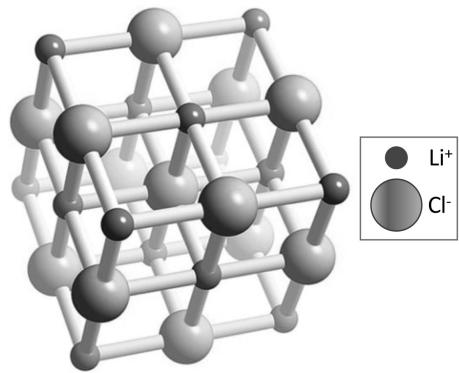
Explicad a qué tipo de enlace corresponden estas imágenes (A y B) y justificad la geometría o estructura de estos compuestos y qué tipo de enlace predomina en ellos, utilizando los datos de electronegatividad de la tabla adjunta.
Representad las estructuras de Lewis del y del .
Justificad, mediante la teoría de repulsión de los pares de electrones de la capa de valencia (RPECV), las geometrías de las moléculas de cloruro de berilio (imagen A) y del agua, y razonad si se trata de moléculas polares o apolares.
Los valores de las primeras energías de ionización del litio y del berilio son, respectivamente, y . Razonad por qué las energías de ionización tienen signo positivo.
Indicad a qué grupo y periodo pertenece cada uno de los elementos.
Explicad, a partir de su configuración electrónica y el modelo atómico de cargas eléctricas, por qué es mayor la energía de ionización del berilio que la del litio.
