1Sèrie 5
2 puntosSèrie 5
El ibuprofeno, que podemos representar como , es un antiinflamatorio que se utiliza para combatir el dolor y los estados febriles. Es un ácido monoprótico débil que contiene un solo grupo ácido carboxílico (—COOH) en su molécula. Hemos preparado en el laboratorio una solución acuosa de este ácido y, al medir el pH, obtenemos un valor de a .
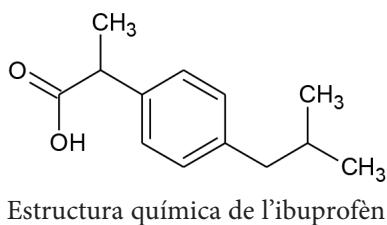
Calcule la constante de acidez, , del ibuprofeno a .
Queremos valorar la solución acuosa de ibuprofeno con , pero en el laboratorio solo disponemos de una solución de . Calcule qué volumen de esta solución necesitamos para preparar de una solución de . Explique cómo la prepararía en el laboratorio e indique el material que utilizaría. Justifique si podemos emplear el rojo de metilo como indicador para detectar el punto final de esta valoración ácido-base.
