Escriba la reacción de precipitación del yoduro de plomo(II) y explique razonadamente, realizando los cálculos necesarios, si precipitará yoduro de plomo(II) cuando mezclemos de disolución acuosa de yoduro de potasio con de disolución acuosa de nitrato de plomo(II) , a . Suponga que los volúmenes son aditivos.
QuímicaCataluñaPAU 2016Ordinaria
Química · Cataluña 2016
14 ejercicios
Ejercicio 1 · Sèrie 3
1Sèrie 3
2 puntosSèrie 3
El yoduro de plomo(II) () es una sal de color amarillo, bastante insoluble en agua fría, que se puede obtener mezclando disoluciones acuosas de nitrato de plomo(II) () y de yoduro de potasio ().
Explique qué procedimiento seguiría en el laboratorio, mencione qué materiales utilizaría y realice los cálculos necesarios para preparar la disolución acuosa, antes mencionada, de yoduro de potasio a partir del producto sólido.
Ejercicio 1 · Sèrie 5
1Sèrie 5
2 puntosSèrie 5
El ibuprofeno, que podemos representar como , es un antiinflamatorio que se utiliza para combatir el dolor y los estados febriles. Es un ácido monoprótico débil que contiene un solo grupo ácido carboxílico (—COOH) en su molécula. Hemos preparado en el laboratorio una solución acuosa de este ácido y, al medir el pH, obtenemos un valor de a .
Calcule la constante de acidez, , del ibuprofeno a .
Queremos valorar la solución acuosa de ibuprofeno con , pero en el laboratorio solo disponemos de una solución de . Calcule qué volumen de esta solución necesitamos para preparar de una solución de . Explique cómo la prepararía en el laboratorio e indique el material que utilizaría. Justifique si podemos emplear el rojo de metilo como indicador para detectar el punto final de esta valoración ácido-base.
Ejercicio 2 · Sèrie 3
2Sèrie 3
2 puntosSèrie 3
La figura siguiente representa el diagrama de fases del agua.
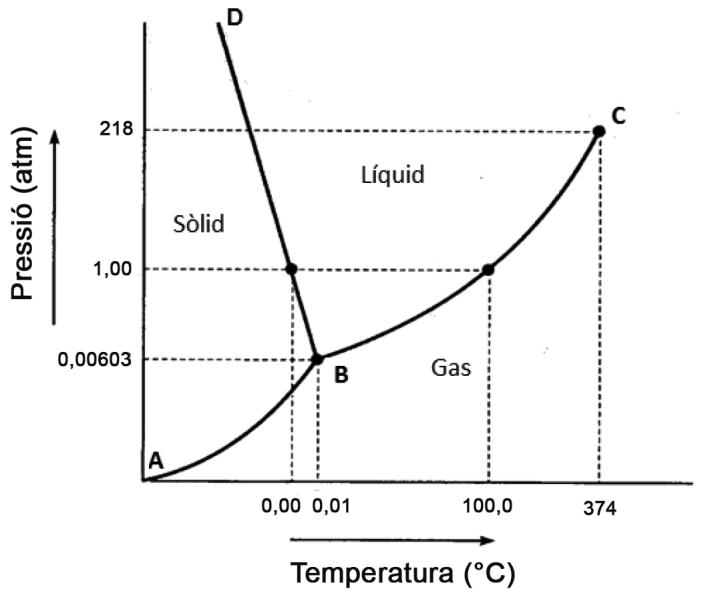
Dé el nombre y la definición de los puntos B y C, y de las líneas AB, BC y BD.
¿Cuál es el estado físico del agua a y ? Partiendo de estas condiciones de temperatura y presión, calentamos el agua a presión constante hasta . Explique qué le sucede a medida que aumenta la temperatura. Nombre todos los cambios de fase que tienen lugar. Dibuje, en el cuaderno de respuestas, el diagrama de fases e indique los estados inicial y final, y la línea de calentamiento.
Ejercicio 2 · Sèrie 5
2Sèrie 5
2 puntosSèrie 5
La electrólisis es un proceso en el que se aporta energía eléctrica para que se produzca una reacción redox no espontánea. Mediante la electrólisis de una solución acuosa de cloruro de cobre(II), empleando dos electrodos inertes de grafito, se obtiene en el ánodo y se deposita en el cátodo.
Escriba las semirreacciones que tienen lugar en el ánodo y en el cátodo, indique la polaridad de los electrodos y diga si la semirreacción es de oxidación o de reducción. Escriba la ecuación química global que se produce en el proceso de electrólisis.
En el laboratorio llevamos a cabo la electrólisis de una solución acuosa de cloruro de cobre(II) durante , empleando una corriente continua de , y obtenemos de . Calcule la masa atómica del cobre.
Ejercicio 3 · Sèrie 3
3Sèrie 3
2 puntosSèrie 3
Por electrólisis de una disolución acuosa de cloruro de oro(III) (), se obtiene cloro gaseoso y se deposita oro.
Escriba las semirreacciones que tienen lugar en el ánodo y en el cátodo, y la reacción global. Realice un esquema de la celda electrolítica, e indique el electrodo positivo y el negativo, el ánodo y el cátodo, el movimiento de los iones en el interior de la celda y el de los electrones por el circuito exterior.
Calcule el número de átomos de oro y el número de moléculas de cloro que se obtienen cuando un mol de electrones ha pasado por el circuito.
Ejercicio 3 · Sèrie 5
3Sèrie 5
2 puntosSèrie 5
Muchos ésteres tienen un aroma característico y, por esta razón, se utilizan frecuentemente como aromatizantes artificiales y aditivos alimentarios. Uno de estos ésteres es el butanoato de etilo, llamado habitualmente butirato de etilo, que tiene un aroma parecido al de la piña tropical. Lo podemos obtener por reacción entre el ácido butanoico y el etanol, de acuerdo con la ecuación química siguiente:
La constante de equilibrio, , de esta reacción tiene un valor de a la temperatura de . Un recipiente contiene una mezcla formada por de ácido butanoico, de etanol, de butanoato de etilo y de agua.

Justifique, a partir de los cálculos necesarios, por qué esta mezcla no está en equilibrio a . ¿Cuáles serán las cantidades (en moles) de cada compuesto cuando la mezcla alcance el equilibrio?
Queremos mejorar el rendimiento de la reacción de obtención del éster y nos proponen aplicar alguna de las tres estrategias siguientes: aumentar la presión, añadir una sustancia higroscópica o añadir más cantidad de alcohol. Explique razonadamente si con cada una de las estrategias conseguiremos el objetivo que nos proponemos o no.
Ejercicio 4 · Sèrie 3
4Sèrie 3
2 puntosSèrie 3
Elija UNA cuestión entre la 4 y la 5.
El consumo de sustancias estupefacientes conlleva un grave problema de salud pública. Estas sustancias permanecen acumuladas en diferentes partes del cuerpo durante un cierto tiempo, que varía desde días hasta meses. Por ejemplo, podemos detectar la cocaína () y la anfetamina () en el cabello de una persona hasta pasados noventa días de haber consumido mediante la técnica de espectrometría de masas. En la figura siguiente se puede ver el espectro de masas obtenido a partir del cabello de una persona de la cual sospechamos que ha tomado una de estas drogas.
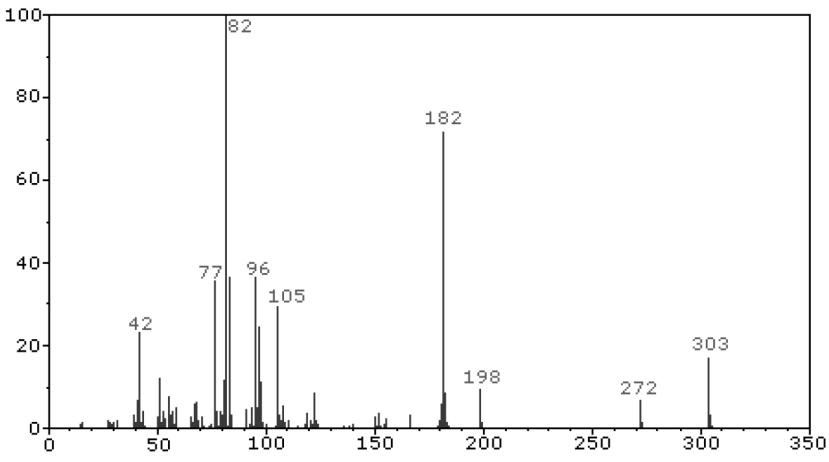
¿Qué magnitud se ha representado en el eje horizontal del gráfico? A partir de las datos experimentales, deduzca si la persona ha tomado cocaína o anfetamina.
A de temperatura y a de presión, la cocaína se encuentra en estado gaseoso. Calcule el volumen molar de la cocaína en estas condiciones de temperatura y presión, suponiendo que se trata de un gas ideal. ¿Qué diferencias hay entre un gas real y un gas ideal?
Ejercicio 4 · Sèrie 5
4Sèrie 5
2 puntosSèrie 5
Elija UNA cuestión entre la 4 y la 5.
El óxido de calcio o cal viva es un compuesto inorgánico muy importante en el ámbito industrial. En el control de la contaminación se utiliza para eliminar el dióxido de azufre generado en algunas centrales eléctricas mediante la reacción siguiente:
En una central eléctrica se eliminan, cada minuto, de dióxido de azufre. Calcule el calor que se liberará por minuto en el proceso de eliminación del dióxido de azufre con cal viva si se produce a una presión constante de y una temperatura de .
En el caso de que el proceso se produjera a volumen constante, justifique si se liberaría una cantidad de calor superior, inferior o igual.
Ejercicio 5 · Sèrie 3
5Sèrie 3
2 puntosSèrie 3
Elija UNA cuestión entre la 4 y la 5.
Para calcular la energía reticular del cloruro de magnesio () es necesario conocer los datos termodinámicos que aparecen en la tabla siguiente:
| Magnitudes en condiciones estándar y a 25 °C | Valor (kJ mol-1) |
| Energía de sublimación del magnesio | 146,3 |
| Primera energía de ionización del magnesio | 736,3 |
| Segunda energía de ionización del magnesio | 1 448,4 |
| Energía de disociación del cloro gaseoso | 242,6 |
| Afinidad electrónica del cloro | -364,5 |
| Variación de entalpía de formación del cloruro de magnesio | -641,2 |
Dibuje el diagrama de entalpías del cloruro de magnesio (ciclo de Born-Haber) y calcule la energía reticular de esta sal a .
Explique justificadamente si el valor absoluto de la energía reticular del cloruro de magnesio es mayor o menor que el de la energía reticular del cloruro de calcio ().
Ejercicio 5 · Sèrie 5
5Sèrie 5
2 puntosSèrie 5
Elija UNA cuestión entre la 4 y la 5.
El biogás es una mezcla de metano y dióxido de carbono que podemos obtener a partir de las reacciones metabólicas de las bacterias metanógenas. Estas bacterias llevan a cabo diversas reacciones para descomponer la materia orgánica, la última de las cuales es la transformación siguiente del ácido acético:
Una granja se plantea instalar una planta de obtención de biogás a partir de ácido acético y duda de la espontaneidad de este proceso. A partir de los cálculos necesarios, indique si esta reacción de obtención de biogás es espontánea en condiciones estándar y a .
Para controlar el proceso de obtención del biogás hemos registrado el espectro de masas de uno de los tres compuestos que intervienen en la reacción. ¿Qué magnitud se representa en el eje de las abscisas de un espectro de masas? Identifique el compuesto e indique a qué pueden ser debidos los tres picos de mayor intensidad que aparecen en el espectro.
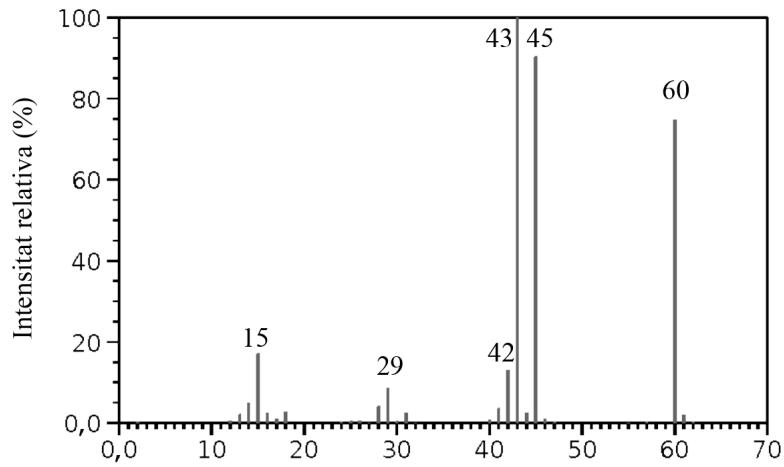
Ejercicio 6 · Sèrie 3
6Sèrie 3
2 puntosSèrie 3
Elija UNA cuestión entre la 6 y la 7.
La síntesis del amoníaco se produce por reacción entre el nitrógeno y el hidrógeno, según la ecuación química siguiente:
Introducimos de nitrógeno y de hidrógeno en un reactor cerrado de . Cuando calentamos la mezcla gaseosa a , observamos que la presión en el equilibrio es de . Calcule, a :
El porcentaje de nitrógeno que ha reaccionado una vez se ha alcanzado el equilibrio.
La constante de equilibrio en concentraciones .
Ejercicio 6 · Sèrie 5
6Sèrie 5
2 puntosSèrie 5
Elija UNA cuestión entre la 6 y la 7.
Conocer la velocidad de una reacción química y determinar de qué depende es muy útil cuando se diseña el proceso de fabricación de una sustancia nueva. Los ingenieros químicos deben buscar, en cada caso, cómo se puede mejorar el rendimiento de una reacción, pero también cómo se puede acelerar la reacción. En un reactor, a volumen constante y a la temperatura de , se ha realizado un estudio de la cinética de la reacción siguiente:
Las datos experimentales obtenidas demuestran que la reacción es de primer orden respecto de A y de orden cero respecto de B.
Escriba la ecuación de velocidad de la reacción. Calcule la constante de velocidad de esta reacción a si, para una concentración inicial del reactivo A de y del reactivo B de , la velocidad inicial de la reacción es . ¿La velocidad de la reacción se mantendrá, disminuirá o aumentará cuando hayan transcurrido unos cuantos minutos después del inicio de la reacción? Justifique la respuesta.
¿Qué es un catalizador? Explique cómo actúa un catalizador en una reacción química a partir del modelo del estado de transición.
Ejercicio 7 · Sèrie 3
7Sèrie 3
2 puntosSèrie 3
Elija UNA cuestión entre la 6 y la 7.
La única manera de determinar la ecuación de velocidad de una reacción es realizando experimentos para medir el efecto que produce la variación de concentración de los reactivos sobre la velocidad. A continuación, puede ver una reacción y los resultados obtenidos, a una temperatura determinada, cuando estudiamos su cinética mediante el método de las velocidades iniciales:
| Experimento | [H2] (mol L-1) | [NO] (mol L-1) | Velocidad (mol L-1 s-1) |
| 1 | 2,0 × 10-2 | 2,50 × 10-2 | 4,8 × 10-6 |
| 2 | 2,0 × 10-2 | 1,25 × 10-2 | 1,2 × 10-6 |
| 3 | 4,0 × 10-2 | 2,50 × 10-2 | 9,6 × 10-6 |
Calcule el orden de reacción respecto de cada reactivo y el orden total.
Determine la constante de velocidad de la reacción. A partir de la teoría de las colisiones, explique dos maneras de aumentar la velocidad de esta reacción química.
Ejercicio 7 · Sèrie 5
7Sèrie 5
2 puntosSèrie 5
Elija UNA cuestión entre la 6 y la 7.
Uno de los ríos principales que suministran agua a la ciudad de Barcelona es el río Llobregat. En una analítica rutinaria del agua de este río obtenemos los datos siguientes:
| Parámetros | Valores |
| pH | 7,45 |
| iones cloruro, Cl- (mg L-1) | 298 |
| iones sulfato, SO4 2- (mg L-1) | 207 |
| iones calcio, Ca2+ (mg L-1) | 128 |
| iones magnesio, Mg2+ (mg L-1) | 41,9 |
| iones sodio, Na+ (mg L-1) | 87,4 |
Llenamos un tubo de ensayo, hasta la mitad, con agua del río Llobregat a . A continuación, añadimos, gota a gota, una solución concentrada de hasta que empieza a aparecer un poco de precipitado. Justifique, numéricamente, si este precipitado es o .
Llenamos otro tubo de ensayo, hasta la mitad, con agua del río Llobregat y añadimos, gota a gota, una solución de para aumentar su basicidad y hacer precipitar los hidróxidos metálicos insolubles. Cuando el pH es , empieza a precipitar el hidróxido de calcio. ¿Qué valor tiene la constante del producto de solubilidad de este hidróxido a ?
