Datos generales del examen
2Opción B
2 puntosEl ácido salicílico () es un compuesto que se encuentra presente en muchos productos utilizados en medicina. A una temperatura de , este ácido se descompone y produce fenol () y dióxido de carbono, según la reacción química ajustada siguiente:
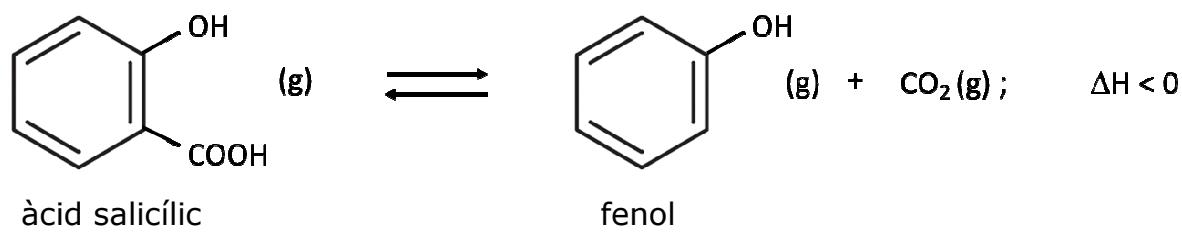
Al laboratorio, introducimos de ácido salicílico en un recipiente de y lo calentamos a . Una vez la mezcla alcanza el equilibrio químico, recogemos el gaseoso obtenido en otro recipiente y comprobamos que este gas ocupa un volumen de , medido a y a . Calcula la constante de equilibrio en concentraciones () correspondiente a la reacción de descomposición del ácido salicílico a .
Si hiciéramos el mismo experimento en un recipiente de , manteniendo la temperatura a , ¿aumentaría la descomposición de ácido salicílico? Justifica la respuesta.
Indica, de forma razonada, si este proceso es espontáneo a cualquier temperatura.
