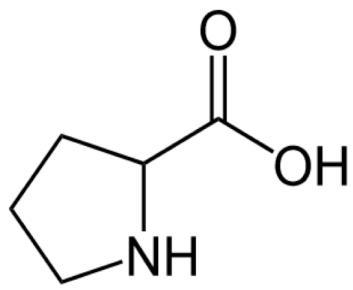
Nombra los grupos funcionales que aparecen en la prolina.
QuímicaBalearesPAU 2022Extraordinaria
Química · Baleares 2022
10 ejercicios
Datos generales del examen
Ejercicio 1 · Opción A
1Opción A
2 puntosEl premio Nobel de Química del año 2021 fue concedido a los investigadores Benjamin List y David WC MacMillan (figura 1) por el desarrollo de un nuevo tipo de catalizadores, los cuales regulan la obtención de moléculas de una forma más eficiente y más respetuosa con el medio ambiente.
En concreto, estos investigadores utilizaron la prolina (figura 2) como catalizador para la producción de nuevos compuestos de gran interés para la industria farmacéutica.

Indica, de forma razonada, la veracidad de la afirmación siguiente: «el uso de un catalizador disminuye la constante de velocidad de la reacción».
Nombra los compuestos siguientes: y .
Ejercicio 1 · Opción B
1Opción B
2 puntosUna industria química obtiene aluminio metálico, , a partir del mineral criolita. Posteriormente, y para protegerlo de la corrosión, la capa superficial de aluminio metálico se transforma en mediante la reacción química no ajustada siguiente:
Ajusta la reacción iónica mediante el método ión-electrón.
Indica cuál es la especie que actúa como oxidante. Justifica la respuesta.
Explica, de forma razonada, por qué en las mismas condiciones ambientales es más fácil que se corroa el magnesio () que el aluminio.
Ejercicio 2 · Opción A
2Opción A
2 puntosEl trihidruro de fósforo, (también conocido como fosfina), a temperatura ambiente es un gas incoloro que se reconoce fácilmente por el fuerte olor a ajo.
Explica la geometría de la molécula de según la teoría de la repulsión de pares electrónicos de la capa de valencia (TRPECV).
Indica si se trata de una molécula polar o apolar. Justifica la respuesta.
Justifica, de forma razonada, por qué el punto de ebullición del amoníaco, (), es más elevado que el punto de ebullición del ().
¿Cuál es el significado del siguiente pictograma, el cual aparece en la ficha técnica del ?

Ejercicio 2 · Opción B
2Opción B
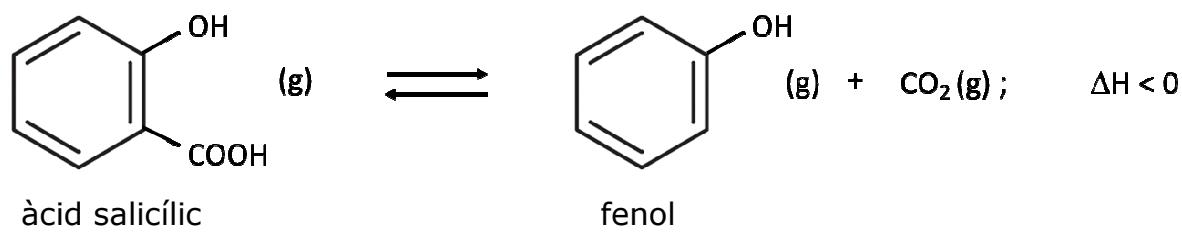
2 puntosEl ácido salicílico () es un compuesto que se encuentra presente en muchos productos utilizados en medicina. A una temperatura de , este ácido se descompone y produce fenol () y dióxido de carbono, según la reacción química ajustada siguiente:
Al laboratorio, introducimos de ácido salicílico en un recipiente de y lo calentamos a . Una vez la mezcla alcanza el equilibrio químico, recogemos el gaseoso obtenido en otro recipiente y comprobamos que este gas ocupa un volumen de , medido a y a . Calcula la constante de equilibrio en concentraciones () correspondiente a la reacción de descomposición del ácido salicílico a .
Si hiciéramos el mismo experimento en un recipiente de , manteniendo la temperatura a , ¿aumentaría la descomposición de ácido salicílico? Justifica la respuesta.
Indica, de forma razonada, si este proceso es espontáneo a cualquier temperatura.
Ejercicio 3 · Opción A
3Opción A
2 puntosEl tolueno () es un hidrocarburo aromático que se utiliza para la producción de explosivos, como el TNT, colorantes, detergentes y otros productos. El tolueno se puede obtener a partir de la deshidrogenación del metilciclohexano () mediante la reacción química siguiente:
En un recipiente de 1 litro, inicialmente vacío, se introducen moles de metilciclohexano y se calientan a , de forma que, una vez alcanzado el equilibrio, hay moles de dihidrógeno dentro de la mezcla gaseosa.
Determina la constante de equilibrio en concentraciones () y la constante de equilibrio en presiones (), ambas a .
¿Qué efecto tendrá sobre la concentración de tolueno presente en la mezcla gaseosa en equilibrio un aumento de la temperatura? Justifica la respuesta.
Ejercicio 3 · Opción B
3Opción B
2 puntosEl ácido sulfúrico () es, probablemente, uno de los reactivos más utilizados en un laboratorio de química.
¿Qué volumen se necesita de una disolución de ácido sulfúrico concentrado, el cual tiene una riqueza del (en peso) y una densidad de , para preparar de una disolución de ácido sulfúrico de concentración ?
Explica el procedimiento y el material de laboratorio necesario para preparar la disolución del apartado anterior.
Ejercicio 4 · Opción A
4Opción A
2 puntosLa industria química produce grandes cantidades de ácido cianhídrico () en todo el mundo. Se utiliza para fabricar explosivos, fibras sintéticas, plásticos, pesticidas, etc.
Una disolución acuosa de este compuesto, a , presenta un .
Calcula la concentración, en mol/L, de esta disolución.
Calcula el grado de disociación del ácido cianhídrico.
Sin necesidad de hacer cálculos numéricos, explica si una disolución de presentará un pH ácido, básico o neutro.
Ejercicio 4 · Opción B
4Opción B
2 puntosEl ácido benzoico () es un ácido carboxílico monoprótico que se utiliza en la elaboración de cosméticos, tintes, plásticos y repelentes de insectos. La constante de acidez () del ácido benzoico, a , presenta un valor de .
En el laboratorio se preparan de una solución acuosa que contiene de ácido benzoico. Calcula el pH de esta disolución a .
Una industria química ha comprado una solución acuosa de ácido benzoico. Para conocer su concentración, se valoran de esta solución con una solución acuosa de hidróxido sódico () , y se consumen de esta base para llegar al punto final de la valoración. Escribe la reacción de neutralización que tiene lugar y calcula la concentración de la solución acuosa de ácido benzoico, expresada en g/L.
Ejercicio 5 · Opción A
5Opción A
2 puntosIndica, de forma razonada, la veracidad de las siguientes afirmaciones relacionadas con la estructura atómica y las propiedades periódicas de los elementos:
El valor del número cuántico principal, , está asociado a la energía y a la forma de un orbital.
El radio del átomo de sodio () es más grande que el radio de su catión ().
La siguiente combinación de números cuánticos corresponde a un electrón del orbital .
El litio () es más electronegativo que el flúor ().
Ejercicio 5 · Opción B
5Opción B
2 puntosDos elementos químicos, A y B, presentan las configuraciones electrónicas siguientes:
Indica, de forma razonada, la posición (grupo y periodo) de cada uno de estos dos elementos en la tabla periódica.
Si se sabe que los valores de las primeras energías de ionización son y , justifica cuál es el valor que corresponde a cada uno de los dos elementos (A y B).
Razona cuál de los dos elementos presenta más tendencia a formar enlaces de carácter metálico.
Explica, de forma razonada, el tipo de enlace que presentará la molécula .
