5
2 puntosElija entre la cuestión 4 y la 5.
El ácido salicílico es un aditivo importante que está presente en muchos productos empleados en medicina. A una temperatura de , este ácido se descompone y produce fenol y dióxido de carbono, según la ecuación química siguiente:
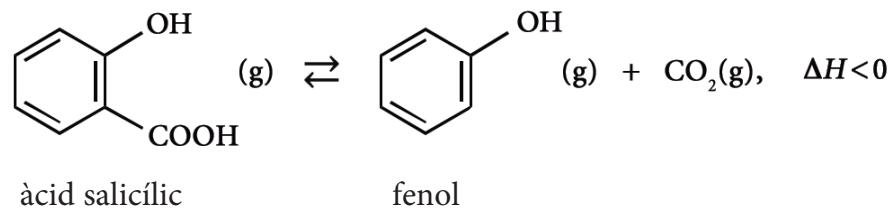
En el curso de un experimento, introducimos de ácido salicílico en un recipiente de y lo calentamos a . Cuando la mezcla alcanza el equilibrio, la enfriamos y, a continuación, recogemos y medimos el gaseoso obtenido; este gas ocupa un volumen de , medido a y a . Calcule la constante de equilibrio en concentraciones () de la reacción de descomposición del ácido salicílico a .
¿Se descompondría más o menos cantidad de ácido salicílico si hiciéramos el mismo experimento en un recipiente de , manteniendo la temperatura a ? ¿Y si hiciéramos el mismo experimento a , manteniendo el volumen del recipiente en ? Justifique las respuestas.
