Calcule la variación de entropía estándar de la reacción de descomposición del agua oxigenada a . Justifique si la reacción es espontánea en condiciones estándar y a .

| Sustancia | |||
| (J K mol) | 205,0 | 109,6 | 70,0 |

Elija entre la cuestión 4 y la 5.
| Color de las radiaciones | Intervalo de Frecuencia de las radiaciones (Hz) |
| violeta | de a |
| azul | de a |
| cian | de a |
| verde | de a |
| amarillo | de a |
| naranja | de a |
| rojo | de a |
Elija entre la cuestión 4 y la 5.
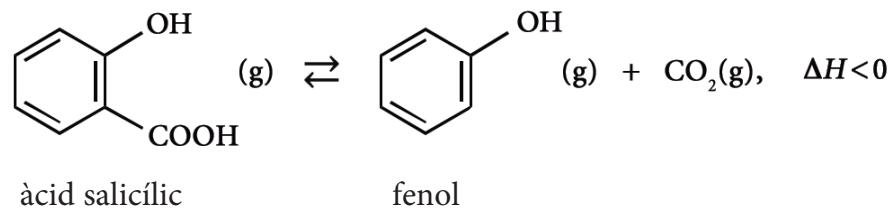
Elija entre la cuestión 6 y la 7.
| Enlace | C-C | C-H | O-H | O=O | C=O |
| Entalpía de enlace, en condiciones estándar y a 298 K (kJ mol) | 348 | 413 | 463 | 498 | 804 |
Elija entre la cuestión 6 y la 7.