3Sèrie 1
2 puntosSèrie 1
La pila de combustible de electrolito polimérico que se muestra en la figura es una pila de combustible típica. El funcionamiento consiste en introducir en la celda hidrógeno y oxígeno gaseosos de manera continuada, a la vez que se elimina el producto de la reacción (agua). Así, se puede generar energía eléctrica mientras se mantiene el suministro de reactivos. Esta pila está formada por dos electrodos recubiertos de platino, que actúa como catalizador, separados por una membrana polimérica que contiene un electrolito y que permite el paso de .
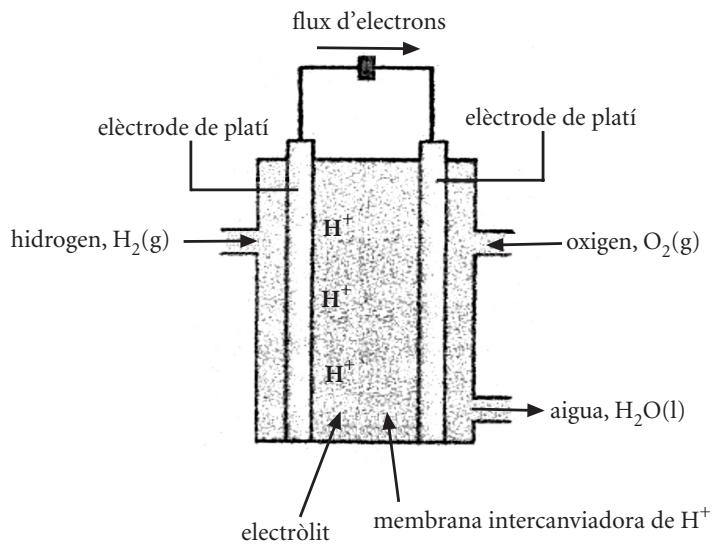
Escriba las semirreacciones anódica y catódica, y la reacción global de la pila de combustible de electrolito polimérico. Indique la polaridad de los electrodos.
La cantidad teórica máxima de energía eléctrica disponible en una pila electroquímica es la variación de energía libre (), mientras que la cantidad máxima de energía liberada cuando se quema un combustible es su variación de entalpía (). Para evaluar una pila de combustible se utiliza el parámetro del valor de eficiencia (), que se define . Calcule la fuerza electromotriz (FEM) y la eficiencia () de la pila de combustible de electrolito polimérico, en condiciones estándar y a .
