Determine la constante de equilibrio en concentraciones () de la reacción de disociación del a .
QuímicaCataluñaPAU 2011Ordinaria
Química · Cataluña 2011
14 ejercicios90 min de duración
Ejercicio 1 · Sèrie 1
1Sèrie 1
2 puntosSèrie 1
Los óxidos de nitrógeno forman parte de la polución de las grandes ciudades debido a la combustión en los motores de explosión. El es incoloro y el es marrón y más tóxico. En una experiencia de laboratorio se introducen de en un recipiente de , y se calientan hasta para provocar la disociación del en . Pasado un cierto tiempo, cuando la mezcla ha alcanzado el equilibrio, se analiza el contenido del recipiente y se encuentra que la cantidad de es .
Si el aire de las grandes ciudades en verano, y en días sin viento, es más marrón que en invierno, justifique si la reacción de disociación del es endotérmica o exotérmica.
Ejercicio 1 · Sèrie 4
1Sèrie 4
2 puntosSèrie 4
Uno de los problemas que tuvieron los químicos del siglo pasado fue la manera de conseguir algún compuesto de nitrógeno a partir del nitrógeno atmosférico, ya que el nitrógeno es un elemento imprescindible en la fabricación de abonos y explosivos. Encontró la respuesta el químico alemán Fritz Haber, quien diseñó un proceso para obtener amoníaco a partir del nitrógeno del aire, en el que ocurre la reacción siguiente:
En un matraz de , a , introducimos de nitrógeno, de hidrógeno y de amoníaco.
Justifique por qué el sistema no está en equilibrio y explique razonadamente hacia dónde se desplazará la reacción.
Una vez alcanzado el equilibrio, ¿obtendremos más amoníaco si disminuimos el volumen del recipiente? ¿Y si añadimos un catalizador? Justifique las respuestas.
Ejercicio 2 · Sèrie 1
2Sèrie 1
2 puntosSèrie 1
La acidez del vinagre proviene del contenido que tiene en ácido etanoico, habitualmente llamado ácido acético, cuya concentración se puede determinar mediante una valoración con hidróxido de sodio.
Escriba la ecuación de la reacción de valoración. Calcule la concentración de ácido acético en el vinagre, expresada en , teniendo en cuenta que en la valoración de de un vinagre comercial se necesitan de una solución de hidróxido de sodio para llegar al punto final.
Explique el procedimiento experimental que seguiría en el laboratorio para llevar a cabo esta valoración, e indique el material y los reactivos que utilizaría.
Ejercicio 2 · Sèrie 4
2Sèrie 4
2 puntosSèrie 4
El tetróxido de dinitrógeno se descompone en dióxido de nitrógeno según la reacción siguiente:
A partir de la figura, conteste razonadamente las cuestiones siguientes.
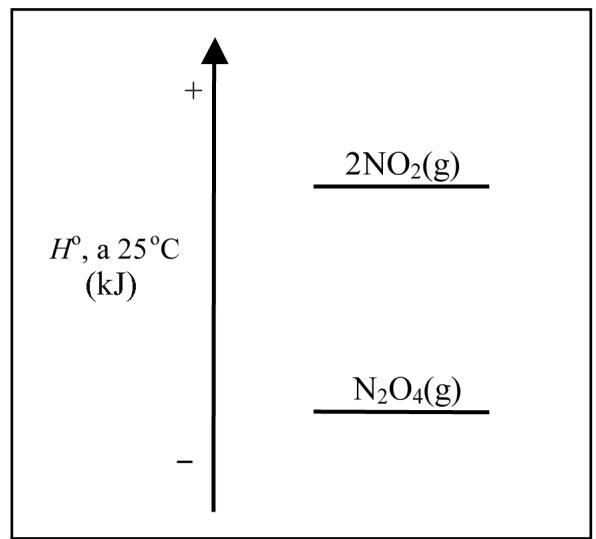
¿Qué signo tendrán la variación de entalpía estándar () y la variación de entropía estándar () de la reacción de disociación del en , a ?
¿Cuándo será espontánea la reacción, a temperaturas altas o a temperaturas bajas?
Ejercicio 3 · Sèrie 1
3Sèrie 1
2 puntosSèrie 1
La pila de combustible de electrolito polimérico que se muestra en la figura es una pila de combustible típica. El funcionamiento consiste en introducir en la celda hidrógeno y oxígeno gaseosos de manera continuada, a la vez que se elimina el producto de la reacción (agua). Así, se puede generar energía eléctrica mientras se mantiene el suministro de reactivos. Esta pila está formada por dos electrodos recubiertos de platino, que actúa como catalizador, separados por una membrana polimérica que contiene un electrolito y que permite el paso de .
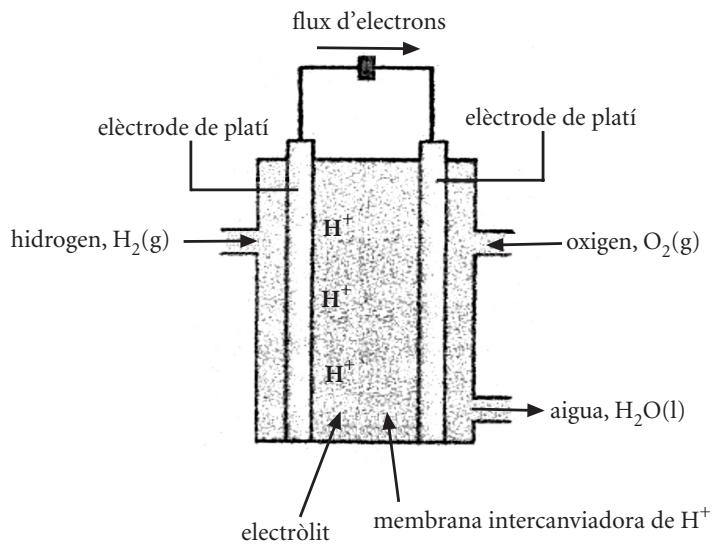
Escriba las semirreacciones anódica y catódica, y la reacción global de la pila de combustible de electrolito polimérico. Indique la polaridad de los electrodos.
La cantidad teórica máxima de energía eléctrica disponible en una pila electroquímica es la variación de energía libre (), mientras que la cantidad máxima de energía liberada cuando se quema un combustible es su variación de entalpía (). Para evaluar una pila de combustible se utiliza el parámetro del valor de eficiencia (), que se define . Calcule la fuerza electromotriz (FEM) y la eficiencia () de la pila de combustible de electrolito polimérico, en condiciones estándar y a .
Ejercicio 3 · Sèrie 4
3Sèrie 4
2 puntosSèrie 4
Conocemos los potenciales estándar de reducción, a , del cobre y del zinc:
Explique razonadamente qué reacción espontánea tendrá lugar en una pila formada por estos dos electrodos, en condiciones estándar y a . Calcule la fuerza electromotriz (FEM) de la pila en estas condiciones.
Queremos comprobar experimentalmente la fuerza electromotriz de esta pila en condiciones estándar y a . Explique cómo la montaría en el laboratorio para hacer la comprobación, e indique el material y los reactivos que utilizaría.
Ejercicio 4 · Sèrie 1
4Sèrie 1
2 puntosSèrie 1
Elija UNA cuestión entre la 4 y la 5.
Uno de los gases más presentes en nuestra vida es el metano, componente principal del gas natural, que es un buen combustible. A partir de las datos de la tabla siguiente, responda a las cuestiones.
| Reacción de combustión | Entalpía de combustión (kJ mol-1) |
| -890,3 | |
| -393,5 | |
| -285,8 |
Imagine que se quiere duchar con el agua a una temperatura de . Teniendo en cuenta que el agua entra en el calentador a y que gastará , diga qué masa de metano hay que quemar, a presión constante, para calentarla.
Escriba la reacción correspondiente a la entalpía estándar de formación del metano, y calcule su valor a .
Ejercicio 4 · Sèrie 4
4Sèrie 4
2 puntosSèrie 4
Elija UNA cuestión entre la 4 y la 5.
El alcohol metílico o metanol, , se utiliza como combustible en las fondues de queso, chocolate o carne. La ecuación de la reacción de combustión del metanol es la siguiente:
A partir de los datos de esta tabla, calcule la entalpía estándar de combustión del metanol a .
| Enlace | Entalpía de enlace en condiciones estándar y a 298K (kJ mol-1) |
| C-H | 414 |
| O-H | 528 |
| C=O | 715 |
| O=O | 498 |
| C-O | 352 |
A partir de las entalpías estándar de formación, se ha calculado la entalpía estándar de combustión del metanol a , y el resultado obtenido es . Calcule el calor que se libera, a presión constante, al quemar de metanol con de oxígeno, en condiciones estándar y a .
Ejercicio 5 · Sèrie 1
5Sèrie 1
2 puntosSèrie 1
Elija UNA cuestión entre la 4 y la 5.
Para calcular la energía reticular del cloruro de sodio () hay que conocer los datos termodinámicos que aparecen en la tabla siguiente:
| Magnitudes termodinámicas | Valor (kJ mol-1) |
| Entalpía de sublimación del Na(s) | 107 |
| Primera energía de ionización del Na | 496 |
| Entalpía de formación del Cl(g) | 122 |
| Afinidad electrónica del Cl | -349 |
| Entalpía de formación del NaCl(s) | -411 |
Explique la diferencia que hay entre los conceptos energía de ionización y afinidad electrónica de un elemento, y entre los conceptos energía reticular y entalpía de formación de un compuesto iónico.
Explique razonadamente, a partir del modelo electrostático del sólido iónico, si la energía reticular del bromuro de potasio será mayor o menor que la del cloruro de sodio.
Ejercicio 5 · Sèrie 4
5Sèrie 4
2 puntosSèrie 4
Elija UNA cuestión entre la 4 y la 5.
El nitrito de sodio () y el benzoato de sodio () son dos sales que se utilizan como conservantes en la industria alimentaria.
Escriba las reacciones que se producen cuando se disuelve nitrito de sodio en agua. Justifique, a partir del modelo de Brønsted y Lowry, si la solución será ácida, neutra o básica.
Si se compara el pH de dos soluciones acuosas, una de nitrito de sodio y la otra de benzoat de sodio, de la misma concentración molar y a la misma temperatura, ¿cuál tendrá el pH más alto? Explique razonadamente la respuesta.
Ejercicio 6 · Sèrie 1
6Sèrie 1
2 puntosSèrie 1
Elija UNA cuestión entre la 6 y la 7.
La reacción en fase gaseosa es uno de los pasos intermedios en la síntesis de abonos nitrogenados. Se trata de una reacción de orden 2 respecto al monóxido de nitrógeno, y de orden 1 respecto al oxígeno.
Escriba la ecuación de velocidad para esta reacción. Indique, razonadamente, las unidades con que se expresan la velocidad y la constante de velocidad de esta reacción.
¿Qué sucede con la velocidad de la reacción si aumentamos la temperatura y mantenemos constante el volumen? ¿Y si aumentamos el volumen y mantenemos constante la temperatura? Justifique las respuestas.
Ejercicio 6 · Sèrie 4
6Sèrie 4
2 puntosSèrie 4
Elija UNA cuestión entre la 6 y la 7.
En el análisis químico, las soluciones acuosas de nitrato de plata, , se suelen utilizar para detectar la presencia de iones cloruro en soluciones problema, debido a la precipitación del cloruro de plata de color blanco.
Tenemos una solución problema de iones cloruro muy diluida (). Si tomamos de esta solución y añadimos de una solución de nitrato de plata, ¿detectaríamos la presencia de cloruro?
En los frascos de nitrato de plata podemos encontrar estos pictogramas de seguridad. ¿Qué significan estos pictogramas? ¿Qué precauciones se deberían tomar en la manipulación de las soluciones de nitrato de plata?


Ejercicio 7 · Sèrie 1
7Sèrie 1
2 puntosSèrie 1
Elija UNA cuestión entre la 6 y la 7.
Para determinar la estructura de las moléculas, la química utiliza diferentes técnicas, como la espectroscopia infrarroja, la resonancia magnética nuclear o la espectrometría de masas. En la figura siguiente, se muestra el espectro infrarrojo (IR) de una molécula:
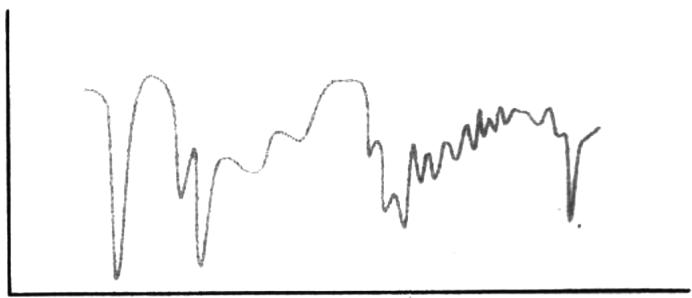
Indique qué magnitud se representa en cada uno de los ejes de un espectro infrarrojo. Explique brevemente el proceso que experimenta un compuesto químico cuando es irradiado con radiación infrarroja.
Considere las sustancias químicas siguientes: , , , . Indique qué compuesto o compuestos no producen ningún pico en un espectro infrarrojo y cuál produce más. Justifique las respuestas.
Ejercicio 7 · Sèrie 4
7Sèrie 4
2 puntosSèrie 4
Elija UNA cuestión entre la 6 y la 7.
El proceso de pirólisis del etanal, a , produce la descomposición de este aldehído en metano y monóxido de carbono, según la ecuación siguiente:
Se ha estudiado la cinética de esta reacción, a , siguiendo la variación de la presión total del reactor con el tiempo. A partir de los datos experimentales obtenidos, y haciendo el tratamiento matemático adecuado, se encuentra la relación siguiente entre la velocidad de la reacción () y la concentración de reactivo:
en la que la velocidad se expresa en y la concentración de etanal, en .
¿Cuál es el orden de la reacción y el valor de la constante de velocidad de la reacción de pirólisis del etanal, a ? Explique razonadamente las respuestas.
Dibuje, de manera aproximada, el perfil de esta reacción en un diagrama de la energía en función de la coordenada de reacción, suponiendo que la reacción se lleva a cabo en una sola etapa, e indique dónde se encuentran las magnitudes de la energía de activación y de la entalpía de reacción. ¿Cómo cambiaría este dibujo si en la reacción de pirólisis se empleara un catalizador? Justifique la variación de la velocidad de la reacción en presencia de un catalizador a partir del modelo del estado de transición.
