¿Qué volumen deberemos tomar de la disolución comercial?
QuímicaBalearesPAU 2011Extraordinaria
Química · Baleares 2011
10 ejercicios
Ejercicio 1 · Opción A
1Opción A
2 puntosLa para la disociación del tetraóxido de nitrógeno a es igual a . Calcula a esta temperatura la concentración de en equilibrio con de existentes en un recipiente de de capacidad. Determina la presión de la mezcla gaseosa.
Ejercicio 1 · Opción B
1Opción B
2,5 puntosSe desea preparar un litro de una disolución de ácido nítrico a partir de un ácido nítrico comercial de densidad y de pureza en peso.
Explica el procedimiento que seguirías para hacer la preparación y nombra el material necesario.
Ejercicio 2 · Opción A
2Opción A
2 puntosLa hidrazina es un combustible para cohetes que al reaccionar espontáneamente con oxígeno genera vapor de agua y nitrógeno gaseoso. Calcula:
El calor de combustión de este proceso.
El calor liberado a presión constante, si en la combustión anterior se utilizan de hidrazina.
Ejercicio 2 · Opción B
2Opción B
2 puntosIndica, razonadamente, si las siguientes afirmaciones son verdaderas o falsas:
La fermentación es un proceso en el cual azúcares y carbohidratos se transforman en metanol y dióxido de carbono.
La capa de ozono de la estratosfera es muy beneficiosa porque deja pasar la luz ultravioleta.
Nunca se deben calentar disoluciones dentro de recipientes cerrados.
Al preparar una disolución acuosa de ácido sulfúrico, se debe adicionar el agua sobre el ácido.
Ejercicio 3 · Opción A
3Opción A
2 puntosUn recipiente contiene de metanol. Razona todas las respuestas.
Calcula el número de moléculas que contiene.
Calcula el número de átomos de hidrógeno que contiene.
Indica la geometría de la molécula, su polaridad y el tipo de interacción intermolecular presente en el metanol líquido.
Indica si el punto de ebullición del etanol será mayor o menor que el del metanol.
Ejercicio 3 · Opción B
3Opción B
1 puntoUnos científicos de la Universidad de Reims han publicado recientemente (J. Agric. Food Chem., 2010, 58, pág. 8768-8775) un estudio sobre las condiciones idóneas para servir el champán, incidiendo en la forma de la copa, la temperatura del champán, y la forma de servirlo (con la copa recta o con la copa inclinada). En el gráfico se representa la concentración de dióxido de carbono disuelto en función de la temperatura.
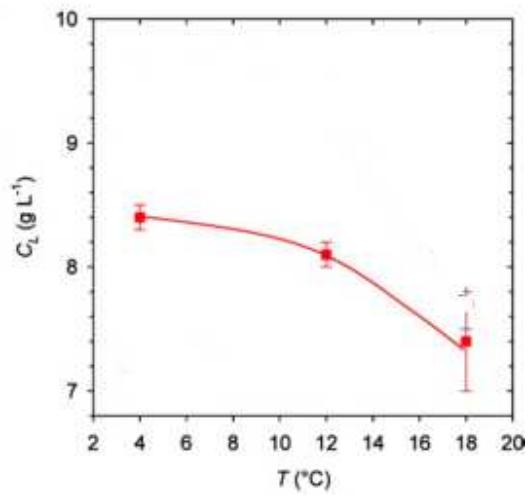
¿Qué conclusión sobre la temperatura óptima para servir el champán puedes obtener en función de estos resultados?
A , ¿cuál es la masa de dióxido de carbono disuelto en una copa de ?
Ejercicio 4 · Opción A
4Opción A
2 puntosExplica razonadamente:
Si se produce alguna reacción al añadir limaduras de cobre a una disolución de sulfato de manganeso (II).
¿Y si añadimos plata metálica a la disolución de sulfato de manganeso (II)?
Si la plata y el manganeso reaccionarán con una disolución de ácido clorhídrico .
Ejercicio 4 · Opción B
4Opción B
2,5 puntosDisponemos de de una disolución acuosa de hidróxido de litio de densidad y con una fracción molar del hidróxido de . Calcula:
La concentración de la disolución en % en peso.
La molaridad de la disolución.
Los gramos de agua que se deberán añadir a la disolución para que la fracción molar en hidróxido sea de .
Ejercicio 5 · Opción A
5Opción A
2 puntosResponde, razonadamente, si son ciertas o no las afirmaciones siguientes:
Hay sales que al disolverse en agua forman disoluciones de pH ácido.
La mezcla equimolecular de un ácido débil y su base conjugada siempre tiene un pH neutro.
Una disolución de tiene un pH de .
El enlace por puente de hidrógeno presente entre las moléculas de metano permite explicar que sea un gas a temperatura ambiente.
Ejercicio 5 · Opción B
5Opción B
2 puntosIndica razonadamente si las siguientes disoluciones son ácidas, básicas o neutras:
de ácido clorhídrico y de hidróxido sódico . Calcula el pH.
de ácido acético y de hidróxido sódico .
de nitrato sódico .
