QuímicaCastilla-La ManchaPAU 2017Ordinaria
Química · Castilla-La Mancha 2017
10 ejercicios
Ejercicio 1 · Opción A
1Opción A
3 puntosCompleta las siguientes reacciones, nombra reactivos y productos e indica de qué tipo son:
Reacción del benceno con ácido nítrico.
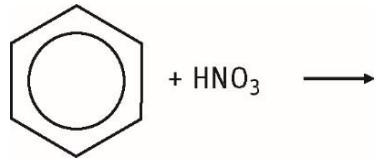
Ejercicio 1 · Opción B
1Opción B
3 puntosEl pH medido en una botella de amoníaco doméstico es . La etiqueta de dicha botella indica que la densidad de la disolución de este amoníaco comercial es g/mL. A partir de estos valores, calcula:
La concentración del amoníaco en la disolución expresada en % en volumen.
El grado de ionización del mismo.
¿Cuál será el pOH que mediremos si diluimos mL del amoníaco comercial con mL de agua?
Ejercicio 2 · Opción A
2Opción A
3 puntos moles de gas fosgeno () puro se introdujeron en un reactor de litros, calentándose entonces éste hasta alcanzar los K de temperatura. Alcanzado el equilibrio, la presión parcial de fue atm. Para el equilibrio calcula:
La constante de presiones .
El número total de moles en el equilibrio.
El grado de disociación del gas fosgeno.
Ejercicio 2 · Opción B
2Opción B
3 puntosPara la reacción de cobre con ácido nítrico (trioxonitrato(V) de hidrógeno) (hidroxidodioxidonitrógeno) que produce nitrato de cobre (II), (trioxonitrato(V) de cobre(II)) (trioxidonitrato de cobre), monóxido de nitrógeno y agua.
Ajusta la ecuación iónica y molecular por el método del ion-electrón.
Señala el oxidante y el reductor.
¿Cuántos gramos de ácido nítrico son necesarios para obtener L de óxido de nitrógeno medidos en condiciones normales?
Ejercicio 3 · Opción A
3Opción A
2 puntosSólo UNA de las siguientes afirmaciones es CORRECTA. Identifícala razonando tu respuesta.
Los metales son malos conductores de la electricidad.
Todos los compuestos iónicos son sólidos.
La unión de un metal con un no metal se produce por enlace covalente.
Los compuestos iónicos no se disuelven en agua.
Ejercicio 3 · Opción B
3Opción B
2 puntosLos átomos neutros A, B, C y D tienen las siguientes configuraciones electrónicas: ; ; ; .
Indica el grupo y período en el que se encuentran.
El nombre y símbolo de cada elemento.
Ordénalos, razonadamente, de mayor a menor electronegatividad.
¿Cuál de ellos presentará mayor potencial de ionización?
Ejercicio 4 · Opción A
4Opción A
1 puntoOrdena razonadamente de menor a mayor el pH de las disoluciones M de los siguientes compuestos: (a) ; (b) ; (c) .
Ejercicio 4 · Opción B
4Opción B
1 puntoIndica, razonando la respuesta, si las siguientes reacciones orgánicas son de adición, eliminación o sustitución.
Obtención de alquenos a partir de alcoholes.
Obtención de derivados halogenados a partir de alquenos.
Obtención de un derivado halogenado a partir de un alcano.
Ejercicio 5 · Opción A
5Opción A
1 puntoSupón una celda voltaica espontánea (pila). Explica razonadamente si las siguientes afirmaciones son ciertas o falsas:
Los electrones se desplazan del cátodo al ánodo.
Los electrones atraviesan el puente salino.
La reducción tiene lugar en el electrodo positivo.
Ejercicio 5 · Opción B
5Opción B
1 puntoEn los siguientes sistemas en equilibrio, predice razonadamente el cambio que se produciría en cada uno de ellos al aumentar la temperatura.
