Ajuste por el método del ion-electrón la reacción de oxidación-reducción en su forma iónica e indique qué especie actúa como agente oxidante y cuál como agente reductor.
QuímicaLa RiojaPAU 2016Ordinaria
Química · La Rioja 2016
10 ejercicios90 min de duración
Ejercicio 1 · Opción A
1Opción A
2 puntosEl ácido oxálico, , se transforma en dióxido de carbono gaseoso cuando reacciona con permanganato potásico, que se transforma en manganeso(II), en medio ácido, según la siguiente ecuación iónica:
Calcule el volumen de disolución de permanganato potásico necesario para oxidar de ácido oxálico.
Determine el volumen de dióxido de carbono que se forma, medido en condiciones normales.
Ejercicio 1 · Opción B
1Opción B
2 puntosDadas las siguientes moléculas: y (C átomo central)
Represente sus estructuras de Lewis.
Indique razonadamente cuál es su geometría.
Indique razonadamente cuál es la hibridación del átomo de O en la primera y de C en la segunda.
Razone sobre la polaridad de los enlaces y de cada una de las moléculas.
Ejercicio 2 · Opción A
2Opción A
2 puntosEn cada uno de los siguientes pares de átomos o iones, indique, razonando su respuesta, cuál de las dos especies tiene mayor radio:
El elemento de o su ion más probable.
El elemento de o el de .
El elemento de o su ion más probable.
El elemento de o el de .
Ejercicio 2 · Opción B
2Opción B
2 puntosSe mezclan de una disolución de sulfato de talio(I) con de disolución de cloruro potásico , tras lo que se observa la aparición de un precipitado de cloruro de talio(I), tal como indica la reacción:
¿Cuál es el reactivo limitante en esta reacción?
Determine la masa de cloruro de talio(I) obtenida suponiendo que precipita todo lo que se forma.
Calcule la molalidad de la disolución de sulfato de talio(I) sabiendo que su densidad es .
Ejercicio 3 · Opción A
3Opción A
2 puntos¿Qué condición se debe cumplir para que una reacción sea espontánea?
Indique qué valores deben de tener y para que una reacción sea espontánea a cualquier temperatura y cuáles deben de tener para que no sea espontánea nunca.
En los demás casos posibles, ¿Cómo influye la temperatura?
Ejercicio 3 · Opción B
3Opción B
2 puntosIndique cuáles son los factores que afectan a la velocidad de una reacción y describa brevemente cómo influye cada uno de ellos en la velocidad.
Ejercicio 4 · Opción A
4Opción A
2 puntosEn un recipiente cerrado de de capacidad que contiene de un gas A y de otro gas B se calienta hasta que se alcanza el siguiente equilibrio:
Una vez alcanzado el equilibrio a esa temperatura, la mezcla de gases contiene de C.
Calcule las concentraciones de cada una de las especies presentes en el equilibrio.
Determine el valor de la constante de equilibrio a esa temperatura.
Explique razonadamente en qué sentido se desplazará el equilibrio si se añade más cantidad de B.
Explique razonadamente en qué sentido se desplazará el equilibrio si se reduce el volumen del recipiente.
Explique razonadamente en qué sentido se desplazará el equilibrio si se aumenta la presión de D.
Ejercicio 4 · Opción B
4Opción B
2 puntosDetermine el pH de una disolución preparada disolviendo de hidróxido de sodio en de agua.
Si a esta disolución se le añaden de disolución de ácido clorhídrico , ¿cuál será el nuevo pH?
Calcule el volumen de disolución de ácido clorhídrico necesario para neutralizar el hidróxido sódico.
Ejercicio 5 · Opción A
5Opción A
2 puntosFormule o nombre correctamente los siguientes compuestos:
Sulfuro de amonio
Ácido permangánico
Ácido 2-etil-3-metilpentanoico
Ejercicio 5 · Opción B
5Opción B
2 puntosIndique el tipo de isomería que existe en los siguientes pares de compuestos:
Isomería geométrica (cis-trans) entre los compuestos mostrados en la imagen.
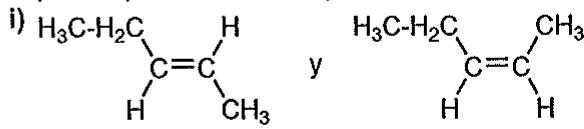
y
¿Qué condición se debe cumplir para que un compuesto orgánico presente isómeros ópticos? ¿Qué otro nombre recibe esta isomería? ¿En qué se diferencia una pareja de isómeros ópticos? Dé un ejemplo de un compuesto que presente este tipo de isomería.
