Se trata de un elemento oxidante.
QuímicaMurciaPAU 2013Ordinaria
Química · Murcia 2013
12 ejercicios
Ejercicio 1 · Opción A
1Opción A
1,5 puntosPonga un ejemplo de sólido covalente y otro de otra especie que en las condiciones adecuadas origine un sólido molecular e indique, en dichos ejemplos, el tipo de interacción que se rompe al pasar del estado sólido al líquido.
Ejercicio 1 · Opción B
1Opción B
1,5 puntosLa configuración electrónica de un elemento es . Justificar si las siguientes afirmaciones son verdaderas o falsas.
Es más electronegativo que el cloro.
Ejercicio 2 · Opción A
2Opción A
1,5 puntosConsidere el siguiente diagrama de energía correspondiente a . Justifique:
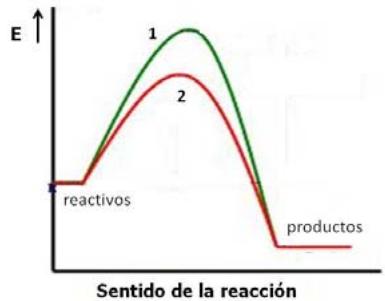
El signo de y si el proceso será espontáneo a temperaturas elevadas.
La posible causa de la diferencia entre las dos curvas. ¿Para cuál de ellas la reacción transcurre a más velocidad?
Ejercicio 2 · Opción B
2Opción B
1,5 puntosDetermine la masa de necesaria para neutralizar de una disolución de un ácido monoprótico débil de que se encuentra disociado un .
Ejercicio 3 · Opción A
3Opción A
1,5 puntosDados los siguientes potenciales normales de reducción elija un agente reductor capaz de reducir a Cd pero no a Mg. Escriba la reacción global correspondiente.
Ejercicio 3 · Opción B
3Opción B
1,5 puntosAjuste la siguiente reacción en forma molecular por el método del ion-electrón:
Ejercicio 4 · Opción A
4Opción A
1,5 puntosNombre o formule los siguientes compuestos: , , , , , bromato de calcio, hidróxido de cinc, p-dietilbenceno, N-metilacetamida, 2,3-dicloro-2-buteno.
Ejercicio 4 · Opción B
4Opción B
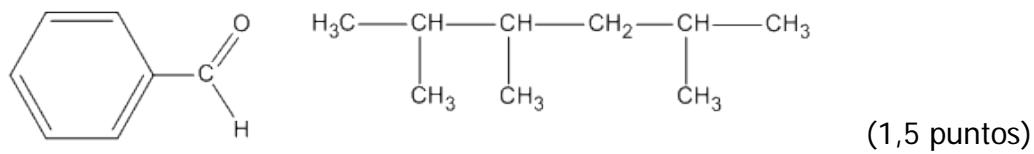
1,5 puntosNombre o formule los siguientes compuestos: cromato de cobre(II), hidruro de berilio, hidrogenosulfuro de bario, etanamina, 1,2-propanodiol, , , y las estructuras mostradas en la imagen.
Ejercicio 5 · Opción A
5Opción A
2 puntosEl fluoruro de sodio reacciona con ácido sulfúrico según:
Calcule:
El volumen de ácido del de riqueza y densidad necesario para atacar de un fluoruro cuya riqueza es del .
La concentración del en términos de y M.
La masa de formada si el rendimiento de la reacción es del .
Ejercicio 5 · Opción B
5Opción B
2 puntosLa reacción de de , de y de origina de , según la reacción:
Calcule:
La masa de reactivo o reactivos que se encuentran en exceso.
El rendimiento de la reacción.
La masa de formada.
Ejercicio 6 · Opción A
6Opción A
2 puntosCuando en un recipiente cerrado se calienta a una mezcla gaseosa formada por de y de se forman en equilibrio de de acuerdo con el proceso:
Calcule la composición en equilibrio si a la misma temperatura se mezclan de y de .
Justifique si las siguientes afirmaciones son verdaderas o falsas:
- Cuando el volumen del recipiente se duplica, la cantidad de reactivos se reduce.
- Cuando aumenta la temperatura disminuye la presión parcial de HI.
- El valor de es independiente de la temperatura.
Ejercicio 6 · Opción B
6Opción B
2 puntosResuelva los siguientes apartados sobre termoquímica:
Calcule la entalpía estándar de formación de la hidracina líquida, , a partir de los siguientes datos:
(1)
(2)
(3)
Calcule la variación de entalpía estándar de la reacción si .
Determine hasta qué temperatura se calentarán de agua, que inicialmente se encuentran a , con el calor desprendido en la reacción de de hidracina y la suficiente cantidad de .
