Calcule el valor de la constante del producto de solubilidad del en agua a .
QuímicaAsturiasPAU 2019Ordinaria
Química · Asturias 2019
10 ejercicios
Ejercicio 1 · Opción A
1Opción A
2,5 puntosDibuje el ciclo de Born-Haber y calcule la energía de red del a partir de los siguientes datos:
Ejercicio 1 · Opción B
1Opción B
2,5 puntosSe mezclan de una disolución acuosa de ácido nítrico, , de , con de una disolución acuosa de ácido clorhídrico, , del en masa y densidad igual a . La mezcla se diluye con agua hasta un volumen final de la disolución de . Calcule el pH de la disolución resultante.
Ejercicio 2 · Opción A
2Opción A
2,5 puntosExperimentalmente se determinó que en de una disolución acuosa saturada de carbonato de calcio, , a , hay de sal disueltos.
Calcule la concentración máxima de que puede estar disuelto en una disolución acuosa que presenta una , a .
Ejercicio 2 · Opción B
2Opción B
2,5 puntosCuando se añade una disolución acuosa de peróxido de hidrógeno, , a una disolución acuosa ácida que contiene bromo disuelto, , se produce una reacción química espontánea. A partir de los valores de los potenciales estándar de reducción, y :
Indique, de forma razonada, la especie química en disolución que experimenta la reacción de oxidación y la que experimenta la reacción de reducción. Escriba y ajuste por el método del ion–electrón la ecuación que representa la reacción química que se produce de forma espontánea. Indique la especie química que actúa como reductor.
Calcule el potencial estándar de la reacción global.
Ejercicio 3 · Opción A
3Opción A
1 puntoDescriba el procedimiento experimental a seguir en el laboratorio para determinar la concentración de peróxido de hidrógeno en un agua oxigenada, mediante la valoración denominada permanganimetría. Indique el material de laboratorio utilizado.
Ejercicio 3 · Opción B
3Opción B
1 puntoPara la valoración de una base fuerte, , con un ácido fuerte, , proponga, de forma razonada, el indicador que utilizaría para identificar el punto de equivalencia y el cambio de color que observaría. Indique el material de laboratorio en el que colocaría el indicador utilizado.
| Indicador | Color (medio ácido) | Intervalo de pH de cambio de color | Color (medio básico) |
| Rojo de metilo | Rojo | 4,8 – 6,0 | Amarillo |
| Tornasol | Rojo | 5,0 – 8,0 | Azul |
| Fenolftaleína | Incoloro | 8,2 – 10,0 | Rosa |
Ejercicio 4 · Opción A
4Opción A
2 puntosIndique, de forma razonada, el carácter ácido, básico o neutro de la disolución acuosa resultante de la neutralización exacta de una disolución acuosa de hidróxido de sodio, , con una disolución acuosa de ácido nitroso, .
Datos
Ajuste, por el método del ion-electrón en medio básico, la siguiente ecuación química:
Ejercicio 4 · Opción B
4Opción B
2 puntosLos siguientes diagramas de orbitales corresponden a especies químicas neutras. Indique los diagramas que son correctos, los que son incorrectos y los que corresponden a estados fundamentales o excitados del átomo neutro. Justifique todas las respuestas.

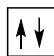
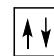
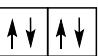
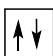
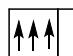

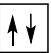
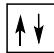
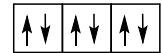
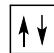

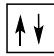
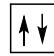
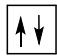
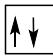
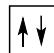
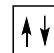
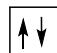
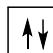
Escriba las configuraciones electrónicas, en estado fundamental, de los elementos X (Z=17) e Y (Z=35). Indique el grupo y periodo de la tabla periódica a los que pertenece cada uno de los elementos. A partir de su posición en la tabla periódica, indique, de forma razonada, el elemento que previsiblemente presentará el valor más elevado de la primera energía de ionización.
Ejercicio 5 · Opción A
5Opción A
2 puntosPara la reacción química elemental , dibuje: i) un perfil energético; ii) un perfil energético en presencia de un catalizador positivo.
Escriba las fórmulas semidesarrolladas de los siguientes compuestos:
i. Ácido 3-bromohexanoico
ii. 2-butino (but-2-ino)
iii. 4-hidroxipentanal
iv. Butanodiona
v. Fenilmetilamina
vi. Acetato de propilo
Ejercicio 5 · Opción B
5Opción B
2 puntosDeduzca, a partir de su estructura molecular, el carácter polar, o no polar, de la molécula , que presenta una geometría molecular triangular.
Datos
- Valores de las electronegatividades (escala de Pauling):
Escriba las fórmulas semidesarrolladas y nombre tres de los isómeros posibles del ácido carboxílico con fórmula molecular .
