Tomamos una muestra de mL de vinagre y la valoramos con una disolución acuosa de hidróxido de sodio () M. El punto final se consigue con mL de disolución básica. Diga, haciendo los cálculos pertinentes, si este vinagre cumple las normas vigentes. ¿La disolución resultante de la operación anterior es ácida, básica o neutra? Justifique la respuesta cualitativamente.
QuímicaCataluñaPAU 2016Extraordinaria
Química · Cataluña 2016
7 ejercicios90 min de duración
Ejercicio 1
1
2 puntosEl vinagre es una disolución acuosa de ácido acético () en la que hay como mínimo g de ácido por cada mL de vinagre. La Oficina del Consumidor decide analizar un vinagre determinado para ver si cumple las especificaciones requeridas.
Explique qué procedimiento seguiría en el laboratorio y qué material utilizaría para llevar a cabo la valoración.
Ejercicio 2
2
2 puntosEl metanol es el alcohol de cadena más corta que podemos formular. En la industria química, la síntesis del metanol se produce por hidrogenación del monóxido de carbono, según la reacción en fase gaseosa siguiente:
A K, los gases de la reacción están en equilibrio y tienen las presiones parciales siguientes: atm para el monóxido de carbono y atm para el metanol. Sabemos que la presión total es de atm.
Calcule la constante de equilibrio en presiones () y la constante de equilibrio en concentraciones () a K.
¿Queremos aumentar la producción de metanol. ¿Lo conseguiremos si añadimos un catalizador a la mezcla gaseosa en equilibrio? ¿Y si aumentamos la presión total? Justifique las respuestas.
Ejercicio 3
3
2 puntosEn la tabla siguiente se relacionan diferentes elementos metálicos y se especifica el color de la luz que emiten cuando son excitados con la llama de un mechero de gas:
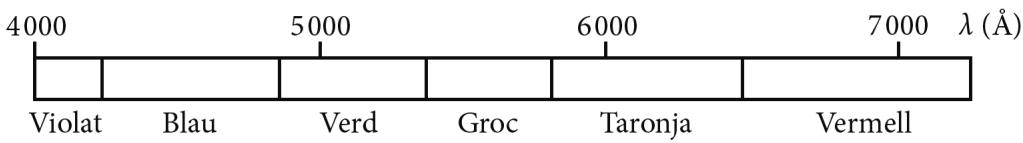
| Elemento | Li | Na | K | Cu |
| Color de la llama | rojo | amarillo | violeta | verde |
Sabemos que la luz emitida por uno de estos elementos corresponde a una transición electrónica de J. ¿De qué elemento se trata? Justifique la respuesta.
Escriba las configuraciones electrónicas del Li, el Na y el K, y compare sus radios atómicos. Justifique la respuesta.
Ejercicio 4
4
2 puntosElija entre la cuestión 4 y la 5.
Para combatir con eficacia el fuego, es necesario saber que la combustión es una reacción química que se produce cuando los vapores que desprende una sustancia combustible se combinan con una gran rapidez con el oxígeno del aire. Esta reacción, con desprendimiento de luz y calor, da lugar al fuego.
| Compuesto | (kJ mol) | (J mol K) |
| -285,8 | 70,0 | |
| -241,8 | 188,0 |
Con los datos de la tabla, calcule la entalpía de vaporización del agua a atm y justifique, a partir del resultado, por qué se utiliza el agua para apagar el fuego. Calcule también el calor necesario para vaporizar kg de agua a una presión constante de atm.
A partir de los datos de la tabla, calcule la temperatura de ebullición del agua a atm de presión.
Ejercicio 5
5
2 puntosElija entre la cuestión 4 y la 5.
Un consumo demasiado elevado de plomo puede provocar la enfermedad llamada saturnismo, que genera anemia en el enfermo porque el plomo en la sangre bloquea la síntesis de la hemoglobina. En las aguas potables, la concentración máxima permitida del ion es .
Escriba el equilibrio de solubilidad del cloruro de plomo(II) y calcule la solubilidad de este compuesto en agua a , expresada en .
¿A partir de qué pH precipitará, a , el hidróxido de plomo(II) en un agua potable que tenga la concentración máxima permitida del ion ?
Ejercicio 6
6
2 puntosElija entre la cuestión 6 y la 7.
La reacción ajustada del ozono con el monóxido de nitrógeno es la siguiente:
Hemos llevado a cabo diferentes experimentos para determinar la velocidad inicial de reacción a diferentes concentraciones y hemos obtenido los resultados siguientes:
| Experimento | [O3] (mol L-1) | [NO] (mol L-1) | Velocidad (mol L-1s-1) |
| 1 | 0,020 | 0,025 | 42,0 |
| 2 | 0,015 | 0,010 | 12,6 |
| 3 | 0,015 | 0,030 | 37,8 |
| 4 | 0,010 | 0,050 | 42,0 |
Calcule el orden de reacción respecto del y respecto del .
Determine el orden total y la constante de velocidad de la reacción. ¿Cómo varía la energía de activación cuando se añade un catalizador al reactor y qué influencia tiene esto sobre la velocidad de reacción?
Ejercicio 7
7
2 puntosElija entre la cuestión 6 y la 7.
En joyería se utiliza frecuentemente el baño de rodio, ya que las joyas recubiertas con este metal brillan mucho y, además, es una alternativa menos cara que el recubrimiento con platino. Queremos recubrir una medalla de plata con rodio mediante electrólisis.
Dibuje el montaje experimental para hacer el recubrimiento de la medalla con una capa de rodio si dispone de una celda electrolítica, de una disolución acuosa de sulfato de rodio(III) () y de un electrodo inerte. Nombre los electrodos e indique su polaridad, y escriba la semirreacción que hace que el rodio se deposite sobre la medalla.
Para obtener un buen recubrimiento necesitamos que se depositen al menos g de rodio. Si hacemos pasar una corriente eléctrica de A durante min, ¿habremos depositado suficiente rodio? Justifique la respuesta.
