Defina afinidad electrónica e indique razonadamente, cuál de estos elementos presentará mayor afinidad electrónica.
QuímicaNavarraPAU 2021Extraordinaria
Química · Navarra 2021
10 ejercicios
Ejercicio 1 · Opción A
1Opción A
2 puntosDetermine la configuración electrónica fundamental de los elementos aluminio, cloro y potasio.
Ordene los elementos aluminio, cloro y potasio de mayor a menor radio atómico justificando su respuesta.
Ejercicio 1 · Opción B
1Opción B
2 puntosDetermine la geometría de las moléculas , y mediante la teoría de repulsión de pares de electrones de la capa de valencia.
Indique la hibridación del átomo central en cada una de ellas.
Justifique si alguna de estas moléculas presenta momento dipolar y señale si en alguna de ellas hay enlaces de tipo .
Ejercicio 2 · Opción A
2Opción A
2 puntosEl fosfato de hierro(III) presenta un producto de solubilidad en agua de .
Indique la ecuación química que describe el proceso de disolución de esta sal en agua, formule la expresión del producto de solubilidad y calcule la solubilidad molar de la sal.
¿Cómo afectará a la solubilidad de la sal la adición de una disolución de cloruro de hierro(III) a la misma disolución?
Ejercicio 2 · Opción B
2Opción B
2 puntosEn un matraz de 2 litros de volumen se introducen moles de nitrógeno y moles de hidrógeno. Cuando se calienta a se alcanza el equilibrio:
y se encuentra que se han formado moles de amoníaco.
Calcule y a la citada temperatura.
Indique justificadamente cómo afecta a la velocidad de la reacción y al equilibrio el hecho de que esta reacción se realice aumentando la temperatura.
Ejercicio 3 · Opción A
3Opción A
2 puntosTenemos dos disoluciones acuosas de la misma concentración, una es de ácido nitroso y la otra de ácido acético.
Escriba los equilibrios de ambos ácidos y justifique cuál de ellos es más fuerte.
Compare los valores de la constante de basicidad de las bases conjugadas de ambos ácidos.
Indique cualitativamente si una disolución de nitrito de amonio tendrá pH ácido, básico o neutro.
Ejercicio 3 · Opción B
3Opción B
2 puntosUna disolución acuosa de ácido acético tiene un .
Halle la concentración inicial de la disolución.
Calcule el volumen de una disolución acuosa de hidróxido de sodio que se necesitará para alcanzar el punto de equivalencia en la valoración de de la citada disolución de ácido acético.
Escriba la ecuación de neutralización del punto anterior y razone cualitativamente si el pH de la disolución en el punto de equivalencia será básico, neutro o ácido.
Ejercicio 4 · Opción A
4Opción A
2 puntosSe realiza en un laboratorio la valoración de de una disolución de permanganato de potasio con una disolución de yoduro de potasio en presencia de ácido sulfúrico, obteniéndose sulfato de manganeso(II), yodo, sulfato de potasio y agua.
Ajuste mediante el método del ion-electrón la reacción que tiene lugar.
Si el punto de equivalencia se encuentra tras añadir de la disolución de yoduro de potasio, calcule la concentración de la disolución de permanganato de potasio.
Ejercicio 4 · Opción B
4Opción B
2 puntosResponda a las siguientes cuestiones sobre procesos redox:
Justifique si se producirá una reacción espontánea al introducir una disolución de nitrato de hierro(II) en un recipiente de aluminio.
Uno de los métodos para prevenir la corrosión del hierro consiste en unirle barras de otro metal, como por ejemplo el magnesio. Explique el fundamento de este proceso.
Ejercicio 5 · Opción A
5Opción A
2 puntosComplete las siguientes reacciones químicas y explique si dichas reacciones son de sustitución, eliminación o adición:
But-1-eno + bromuro de hidrógeno ?
1-yodobutano + hidróxido de potasio ?
Benceno + ácido nítrico, en presencia de ?
Ejercicio 5 · Opción B
5Opción B
2 puntosExplique el concepto de grupo funcional e indique los grupos funcionales presentes en las siguientes moléculas:
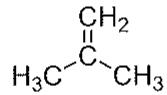
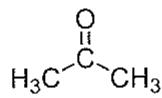
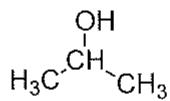
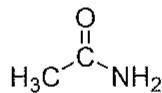
Identifique los grupos funcionales en las moléculas mostradas.
Nombre cada uno de los compuestos anteriores.
