Indique su nombre y símbolo atómico, y el grupo y periodo en que se encuentran.
QuímicaMurciaPAU 2019Ordinaria
Química · Murcia 2019
10 ejercicios
Ejercicio 1 · Opción A
1Opción A
2 puntosDados los elementos A, B y C, con números atómicos: A: ; B: ; C:
¿Cuál será el número de oxidación más importante para los elementos B y C? Indique si estos elementos formarán un compuesto iónico o covalente, y escriba su fórmula.
Escriba la configuración electrónica del elemento C e indique si puede ser un conjunto de números cuánticos válido para su electrón más externo.
Ordene los elementos A, B y C según su radio atómico y explique el origen de esta variación para los elementos A y B.
Ejercicio 1 · Opción B
1Opción B
2 puntosRazone qué sustancia presentará un mayor punto de fusión, el o el .
Razone si las siguientes sustancias sólidas conducen o no la electricidad a temperatura ambiente: , , .
Explique los distintos puntos de ebullición del etano (), dimetil éter () y etanol ().
Ejercicio 2 · Opción A
2Opción A
2 puntosSe dispone de dos disoluciones ácidas de y , ambas de concentración . Calcule:
El pH de la disolución de .
El pH de la disolución de .
Datos
Ejercicio 2 · Opción B
2Opción B
2 puntosCalcule el volumen de una disolución de , de concentración , necesario para neutralizar de una disolución de de concentración .
Datos
- Masas atómicas:
Se dispone de una disolución de y otra de , ambas de concentración . Explique razonadamente cual presentará un valor menor de pH, sabiendo que: y .
Ejercicio 3 · Opción A
3Opción A
2 puntosNombre los siguientes compuestos:
I)
II)
Escriba las fórmulas semidesarrolladas de los siguientes pares de compuestos y explique el tipo de isomería que presentan entre sí:
1) 3,3-Dimetilpentano y 3-metilhexano.
2) Dietil éter y metil propil éter.
3) Butanal y butanona.
4) cis-1,2-Dicloroeteno y trans-1,2-dicloroeteno.
Ejercicio 3 · Opción B
3Opción B
2 puntosFormule o nombre los siguientes compuestos:
1) 2-Metilhex-1-eno
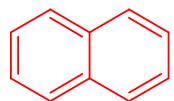
2) Naftaleno
3) Pentano-2,4-diol
4)
5)
Complete las siguientes reacciones orgánicas con los productos mayoritarios esperados, según el tipo de reacción indicado:
1) Sustitución:
2) Adición:
3) Eliminación:
4) Condensación:
5) Combustión:
Ejercicio 4 · Opción A
4Opción A
2 puntosConsidere la siguiente reacción química en fase gaseosa: cuya velocidad de reacción viene dada por la expresión:
Indique cuál es el orden de reacción y las unidades de .
Si en un determinado instante el se está formando a una velocidad de , explique a qué velocidad se estará consumiendo el , en ese mismo instante.
¿Qué le ocurre a la velocidad de reacción () durante el transcurso de la reacción (aumenta, disminuye o permanece constante)? Explique su respuesta.
¿Qué le ocurrirá a la constante de velocidad () si se aumenta la temperatura ( aumenta, disminuye o permanece constante)? Explique su respuesta.
Ejercicio 4 · Opción B
4Opción B
2 puntosEn un recipiente de se introducen de y de , calentándose la mezcla a . Una vez alcanzado el siguiente equilibrio: se analiza la mezcla, encontrándose que quedan de .
Calcule la concentración de cada especie en el equilibrio.
Calcule y a .
Explique cómo afectaría al equilibrio una disminución del volumen del recipiente.
Ejercicio 5 · Opción A
5Opción A
2 puntosDada la siguiente reacción de oxidación-reducción:
Explique cuál es el agente oxidante y cuál el agente reductor.
Ajuste la reacción mediante el método del ion-electrón.
Ejercicio 5 · Opción B
5Opción B
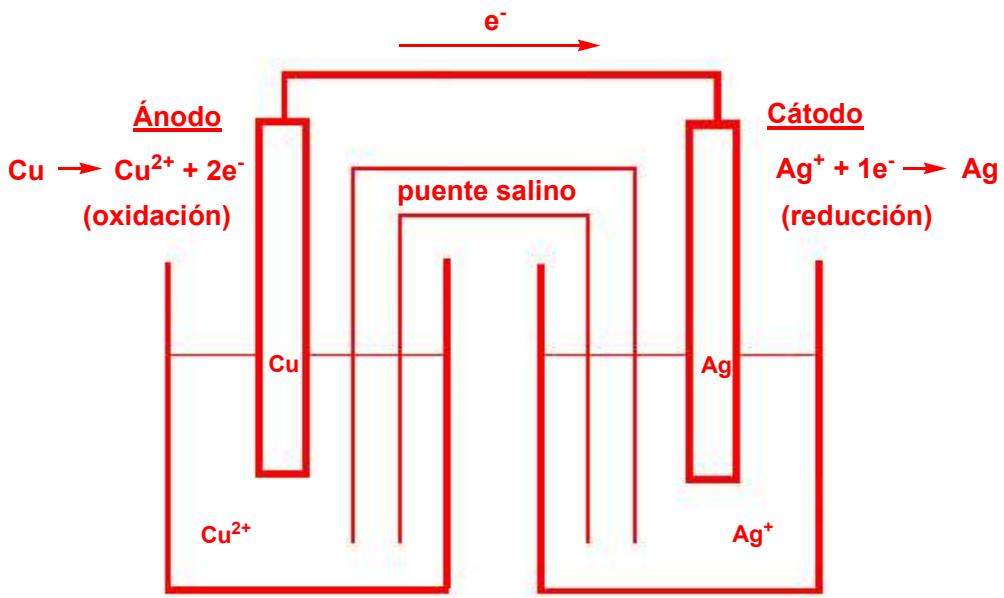
2 puntosConsidere una pila galvánica formada por un electrodo de cobre sumergido en una disolución de y por un electrodo de plata sumergido en una disolución de .
Dibuje un esquema de la pila, con todos los elementos necesarios para su funcionamiento, e indique:
1) Cuál de los electrodos actúa como cátodo y cuál como ánodo.
2) La reacción (oxidación o reducción) que se produce en cada electrodo.
3) El sentido de circulación de los electrones por el circuito externo.
4) La reacción global de la pila.
5) Su fuerza electromotriz.
Explique si la masa de los electrodos varía durante el funcionamiento de la pila.
