Indique el nombre y símbolo atómico del elemento al que corresponde, así como su posición (grupo y periodo) en la Tabla Periódica. ¿Cómo se suele denominar a ese grupo?
QuímicaMurciaPAU 2022Ordinaria
Química · Murcia 2022
10 ejercicios
Ejercicio 1
1
2 puntosDada la siguiente configuración electrónica :
Escriba un posible conjunto de números cuánticos para su electrón diferenciador.
¿Cuántos electrones de valencia, y cuántos electrones desapareados, tendrá este elemento, en su estado fundamental? Justifique brevemente su respuesta.
Razone cuál será el número de oxidación más importante para este elemento.
Indique si este elemento tendrá alta o baja energía de ionización, y si es un metal o no metal.
Ejercicio 2
2
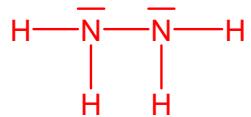
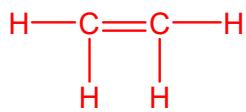
2 puntosConsidere las siguientes sustancias: hidracina () y eteno ()
Represente sus estructuras de Lewis y en base a ellas explique cómo será la geometría en torno a los átomos de N y C, y si estas moléculas son o no planas.
Una de estas dos sustancias se encuentra en estado líquido en el intervalo de temperatura , muy similar al del . Explique de qué sustancia se trata y a qué se debe esta característica.
Una de estas dos sustancias es muy soluble en agua. Explique brevemente cuál será.
Explique brevemente si estas sustancias son o no conductoras de la electricidad.
Ejercicio 3
3
2 puntosSabiendo que la reacción es de primer orden en cada uno de los reactivos:
Escriba la ecuación de velocidad para la reacción, e indique cuál es el orden total de reacción.
Explique si esta reacción puede ocurrir en una sola etapa elemental.
Si en un determinado instante el producto C se está formando a una velocidad de , ¿a qué velocidad se estará consumiendo el producto A, en ese mismo instante?
Indique cómo variarán y si la concentración de A se reduce a la mitad.
Ejercicio 4
4
2 puntosEn un recipiente cerrado y vacío, de de capacidad, se introducen moles de y moles de , dejando evolucionar la mezcla de gases según el siguiente equilibrio:
Explique brevemente en qué sentido se producirá la reacción (no es necesario hacer cálculos).
Si una vez alcanzado el equilibrio hay en la mezcla moles de , calcule el valor de .
Si la mezcla de gases en equilibrio se traslada a un recipiente de de capacidad, explique brevemente si la cantidad de aumentará, disminuirá o permanecerá constante.
Escriba la expresión general de en función de para este equilibrio.
Ejercicio 5
5
2 puntosSe realiza la valoración de de una disolución de con una disolución de :
Escriba la reacción que tiene lugar e indique cómo será el pH en el punto exacto de equivalencia.
¿Qué volumen de la disolución de será necesario para llegar al punto de equivalencia?
Si se utiliza como indicador el rojo de fenol (amarillo en su forma ácida y rojo en su forma básica; intervalo de viraje: pH ), explique brevemente de qué color estará la disolución valorada una vez sobrepasado el punto de equivalencia.
Calcule el pH de la disolución resultante cuando se ha añadido un total de de la disolución de (suponiendo que los volúmenes son aditivos).
Ejercicio 6
6
2 puntosCalcule la masa de , en gramos, necesaria para preparar de una disolución acuosa de de .
Datos
- masas atómicas:
- ()
Sabiendo que el es un ácido muy fuerte, explique brevemente qué base será más débil: o .
Ejercicio 7
7
2 puntosDada la siguiente reacción redox:
Explique brevemente cuál es el agente oxidante y cuál el reductor.
Ajuste la reacción mediante el método del ion-electrón.
Ejercicio 8
8
2 puntosConsidere los siguientes potenciales de reducción (los de los metales no varían con el pH):
¿Cuál de los metales anteriores es tan reductor que reacciona explosivamente con el agua? Escriba la reacción global que tiene lugar.
Según los potenciales dados, ¿debería una cuchara de disolverse en agua (a ) para dar e ? Escriba las semirreacciones de oxidación y reducción que tendrían lugar, calcule el potencial () para la reacción redox y fundamente su respuesta en el signo de dicho valor.
¿De qué metales, de entre los anteriores, tendría que estar hecha una cuchara para no disolverse en ? Explique brevemente su respuesta (no es necesario escribir las reacciones).
Ejercicio 9
9
2 puntosFormule o nombre los siguientes compuestos: a) ; b) anisol; c) .
Escriba las fórmulas semidesarrolladas del siguiente par de compuestos e indique el tipo y subtipo de isomería que presentan entre sí: o-dinitrobenceno y m-dinitrobenceno.
Dado el compuesto :
Nómbrelo.
Indique el tipo y subtipo de isomería que presenta su siguiente par de isómeros:
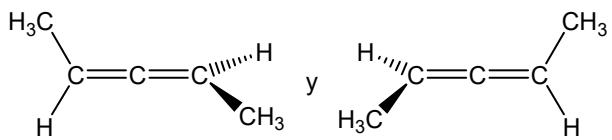
¿Cómo se denomina la siguiente reacción de este compuesto? (una sola palabra es suficiente):
Complete la siguiente reacción de este compuesto:
Ejercicio 10
10
2 puntosFormule o nombre los siguientes compuestos: a) ; b) ácido ftálico.
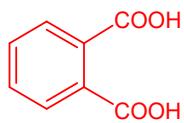
Dado el compuesto :
Nómbrelo.
Explique si puede presentar algún tipo de isomería espacial (geométrica y/u óptica).
Escriba las fórmulas semidesarrolladas de un isómero estructural de función y otro de posición de dicho compuesto.
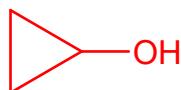
Escriba la ecuación química para la reacción de combustión de este compuesto con .
¿Cómo se denomina la siguiente reacción de este compuesto con ?
