su conductividad en estado sólido (conductor o aislante).
QuímicaLa RiojaPAU 2020Ordinaria
Química · La Rioja 2020
10 ejercicios90 min de duración
Ejercicio 1
1
2 puntosClasifique las siguientes sustancias: , , y , razonando su respuesta, según:
el enlace que presentan (iónico, covalente o metálico). En las covalentes, indique el tipo de fuerzas intermoleculares que existen en cada caso en estado líquido.
su solubilidad en agua (soluble o insoluble).
su estado de agregación a de presión y de temperatura (sólido, líquido o gas).
Ejercicio 2
2
2 puntosEn un experimento de catálisis con el proceso:
se midió la velocidad de la reacción, obteniendo como resultado: . Escriba la velocidad de reacción expresada en términos de cada uno de los reactivos.
Los siguientes datos corresponden a cuatro reacciones químicas de tipo general:
Indique, justificando su respuesta razonadamente:
i) Cuál de ellas es la más rápida.
ii) Cuáles de estas reacciones son espontáneas.
iii) Qué valores de la tabla se pueden modificar mediante la adición de un catalizador.
| (kJ·mol⁻¹) | (kJ·mol⁻¹) | (kJ·mol⁻¹) | |
| Reacción 1 | 1,0 | -2,0 | 0,20 |
| Reacción 2 | 0,5 | 5,0 | -0,80 |
| Reacción 3 | 0,7 | 0,70 | 0,60 |
| Reacción 4 | 1,5 | -0,50 | -0,30 |
Ejercicio 3
3
2 puntosEscriba las fórmulas de las bases conjugadas de los siguientes ácidos y escriba la expresión correspondiente a cada equilibrio ácido/base:
i)
ii)
iii)
iv)
v)
Determine la concentración que debe de tener una disolución acuosa de ácido acético para que el pH de la misma sea .
Datos
Ejercicio 4
4
2 puntosSe somete a electrolisis cloruro de zinc fundido haciendo pasar una corriente de durante cierto tiempo hasta que se depositan de zinc metálico.
Escriba y ajuste las reacciones que tienen lugar en el cátodo y en el ánodo.
Calcule el tiempo necesario para realizar el proceso.
Determine el volumen de gas liberado durante la electrolisis, medido a una temperatura de y a una presión de .
Ejercicio 5
5
2 puntosFormule o nombre correctamente los siguientes compuestos:
i) 4-clorohexa-1,3-dieno
ii) 3-metilhepta-1,4-diol
iii) ácido 3-etilpentanoico
iv) (ver imagen)
v)
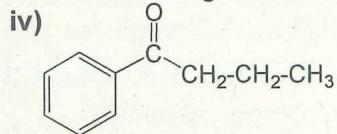
Indique cuáles de los anteriores compuestos presentan isómeros ópticos y señale sus carbonos quirales.
Ejercicio 6
6
2 puntosIndique de manera razonada cuáles de las siguientes configuraciones electrónicas corresponden a un estado fundamental, cuáles a un estado excitado y cuáles son imposibles:
i)
ii)
iii)
iv)
v)
Complete la siguiente tabla:
| Símbolo | N° de protones | N° de neutrones | N° de electrones | Carga |
| 82 | 0 | |||
| 31 | 38 | +3 | ||
| 117 | -1 |
Ejercicio 7
7
2 puntosRazone sobre la veracidad o falsedad de las siguientes afirmaciones:
En la valoración de ácido acético con hidróxido de sodio, en el punto de equivalencia el pH es básico.
El pH de una disolución de bromuro de amonio es mayor que 7.
Si el pH de una disolución de un ácido monoprótico fuerte es , la concentración del ácido está comprendida entre y .
La constante de hidrólisis de una sal formada en la reacción de un ácido débil con una base fuerte es .
Una disolución de nitrato de potasio tiene un pH más bajo que una de acetato de sodio de la misma concentración.
Ejercicio 8
8
2 puntosPara cada una de las siguientes especies: i) , ii) , iii) , iv)
Escriba la ecuación correspondiente al equilibrio de su disolución en agua.
Escriba la expresión que relaciona su constante de equilibrio, , con las concentraciones de los iones presentes en disolución.
Escriba la expresión que relaciona su constante de equilibrio, , con su solubilidad en agua.
Indique de manera razonada cómo afectará a la solubilidad del hidróxido de aluminio en agua la adición de una pequeña cantidad de hidróxido de sodio a una disolución saturada de la primera.
Ejercicio 9
9
2 puntosExplique el efecto que tienen los siguientes cambios sobre el equilibrio:
i) El aumento de la temperatura.
ii) El aumento de la presión.
iii) El aumento de la concentración de dicloro.
iv) La presencia de un catalizador.
Una cierta cantidad de pentacloruro de fósforo se calentó a en un recipiente de , alcanzándose el equilibrio anterior. Determine el valor de y para el mismo a sabiendo que en el equilibrio el recipiente contiene moles de pentacloruro de fósforo, moles de tricloruro de fósforo y moles de dicloro.
Datos
Ejercicio 10
10
2 puntosEscriba los productos de cada una de las siguientes reacciones orgánicas y clasifíquelas según el tipo de reacción del que se trata:
(en medio etanólico)
