Dibuja las estructuras de Lewis de las moléculas y analiza su geometría.
QuímicaPaís VascoPAU 2016Ordinaria
Química · País Vasco 2016
10 ejercicios90 min de duración
Datos generales del examen
- Masas atómicas (u.m.a.): H: 1
- C: 12
- N: 14
- O: 16
- Na: 23
Ejercicio 1 · A · Cuestiones
1A · Cuestiones
2 puntosCuestiones
Considerando las siguientes moléculas: agua, amoníaco y metano.
Analiza la polaridad de las moléculas.
A temperatura ambiente el agua es un líquido, pero el amoníaco es un gas. ¿Por qué?
Ejercicio 1 · A · Problemas
1A · Problemas
2,5 puntosEl calor de combustión del carbono sólido es y el calor de vaporización del agua es .
Escribe las ecuaciones termoquímicas de ambos procesos y representa los diagramas de energía correspondientes.
¿Será espontánea la combustión del carbono sólido a ?
¿Cuántos gramos de hay que quemar para evaporar de agua a ?
Ejercicio 1 · B · Cuestiones
1B · Cuestiones
2 puntosCuestiones
Observando la pila de la figura, responde las siguientes preguntas:
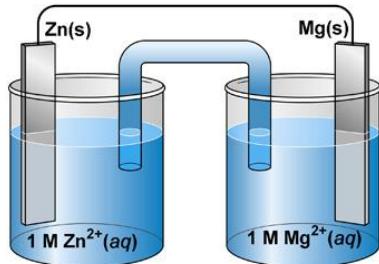
¿Qué procesos tiene lugar en el ánodo y el cátodo de la pila?
Sabiendo que el puente salino contiene nitrato de amonio ¿cómo se moverán dichos iones?
¿En qué sentido se moverán los electrones en el circuito externo?
¿Cuál será la tensión de la pila en condiciones estándar?
Ejercicio 1 · B · Problemas
1B · Problemas
2,5 puntosLas entalpías de formación estándar del y del son, respectivamente, y y el calor de combustión del ácido acético (etanoico) líquido es a .
Escribe las ecuaciones termoquímicas correspondientes a los datos aportados.
Calcula la entalpía estándar de formación del ácido acético.
¿Qué cantidad de calor se intercambiará (debes indicar si se libera o absorbe) cuando se forman de medidos a y al quemar ácido acético (etanoico) líquido?
Ejercicio 2 · A · Cuestiones
2A · Cuestiones
1,5 puntosCuestiones
Dados los potenciales redox: ; ; , indicar de modo razonado:
¿Será espontánea esta reacción química: ?
¿Se obtendrá hidrógeno(g) al mezclar estaño metálico y ? En caso afirmativo, escribe la correspondiente ecuación química.
¿Qué fenómenos químicos tendrán lugar en el cátodo y el ánodo de una pila formada con electrodos de estaño y cobre?
Ejercicio 2 · A · Problemas
2A · Problemas
2,5 puntosEn un matraz de dos litros se introducen moles de pentacloruro de fósforo y se calientan a . El se convierte en vapor y se disocia parcialmente según la siguiente reacción: Sabiendo que en el equilibrio la presión es de , calcular:
La concentración de las diferentes especies en el equilibrio.
El valor de las constantes y a .
Si se aumenta la presión ¿en qué sentido se desplazaría el equilibrio? ¿Cómo afectaría eso al grado de disociación del ?
Ejercicio 2 · B · Cuestiones
2B · Cuestiones
1,5 puntosCuestiones
El etileno reacciona con hidrógeno para formar etano
¿Qué efecto tendrá un aumento de la temperatura sobre la concentración de etileno?
¿Qué efecto tiene una disminución de la presión sobre la cantidad de etano producida?
Ejercicio 2 · B · Problemas
2B · Problemas
2,5 puntosSabiendo que una disolución de amoníaco tiene un de 11
Calcula la concentración de la disolución y el grado de ionización del amoníaco.
¿Cuántos gramos de hay que disolver en de agua para obtener dicho ?
¿Cuántos de harán falta para neutralizar del amoníaco(aq) anterior? ¿Cómo será el en el punto de neutralización? (debes indicar si es ácido, básico o neutro).
Ejercicio 3 · Opción A
3Opción A
1,5 puntosCuestiones
Realiza las siguientes operaciones:
Escribe y nombra un alcohol, un aldehído y una cetona de 4 átomos de carbono que son isómeros entre sí.
Escribe las ecuaciones químicas de deshidratación del 1-butanol y del 2-butanol.
Escribe la ecuación química de síntesis del propanoato de etilo. ¿De qué tipo de reacción se trata?
Ejercicio 3 · Opción B
3Opción B
1,5 puntosCuestiones
Entre estas sustancias: bromuro potásico, fluoruro de hidrógeno, metano y potasio, selecciona:
Una que no es conductora en estado sólido, pero sí fundida.
Una que forma enlaces de hidrógeno intermoleculares.
La que es buena conductora de la corriente eléctrica.
