Escriba las configuraciones electrónicas de los elementos y () en su estado fundamental.
QuímicaAsturiasPAU 2024Extraordinaria
Química · Asturias 2024
10 ejercicios
Ejercicio 1
1
2 puntosResponda, razonadamente, si los siguientes enunciados son verdaderos o falsos:
El y el pueden formar un compuesto iónico.
El y el pueden formar un compuesto covalente.
La estequiometría del compuesto es .
La estequiometría del compuesto es .
Ejercicio 2
2
2 puntosLa fórmula de Rydberg puede utilizarse para obtener un valor aproximado de la primera energía de ionización, , del átomo de hidrógeno: basta, simplemente, con considerar la transición entre y . Calcule, utilizando la fórmula de Rydberg, la primera energía de ionización del átomo de hidrógeno.
Ejercicio 3
3
2 puntosCalcule la constante de equilibrio de la reacción a , sabiendo que al mezclar en un recipiente, a esa temperatura, de y de , se forman, una vez alcanzado el equilibrio (), de y de .
Ejercicio 4
4
2 puntosSe ha determinado, a la misma temperatura, pero en cuatro condiciones iniciales diferentes, la velocidad inicial, , de la reacción
| Exp. | [BrO3-(aq)]0/(mol L-1) | [Br-(aq)]0/(mol L-1) | [H3O+(aq)]0/(mol L-1) | v0/(mol L-1s-1) |
| 1 | 0,10 | 0,10 | 0,10 | 1,2·10-3 |
| 2 | 0,20 | 0,10 | 0,10 | 2,4·10-3 |
| 3 | 0,10 | 0,30 | 0,10 | 3,5·10-3 |
| 4 | 0,20 | 0,10 | 0,15 | 5,5·10-3 |
Calcule el orden de la reacción respecto al .
Calcule el orden de la reacción respecto al .
Calcule el orden de la reacción respecto al .
Calcule el orden total de la reacción.
Calcule la constante cinética.
Escriba la ley de velocidad.
Ejercicio 5
5
2 puntosA través de una disolución acuosa que contiene una sal de , de anión desconocido, pero de estequiometría , se hace circular una corriente eléctrica. Se necesitan para que una corriente de reduzca a cobre metálico todo el contenido en de dicha sal. Calcule la masa molar de la sal.
Ejercicio 6
6
2 puntosEl hidróxido de calcio, , es un sólido poco soluble en agua.
Calcule la energía de Gibbs estándar de reacción, , a , correspondiente al equilibrio entre el hidróxido de calcio sólido y una disolución acuosa saturada de dicho compuesto.
Calcule, a , la constante de equilibrio, (producto de solubilidad), del proceso anterior.
Ejercicio 7
7
2 puntosSe muestra, a continuación, la fórmula estructural desarrollada de la cafeína. Indique, razonadamente, la hibridación de los átomos de carbono , , y .
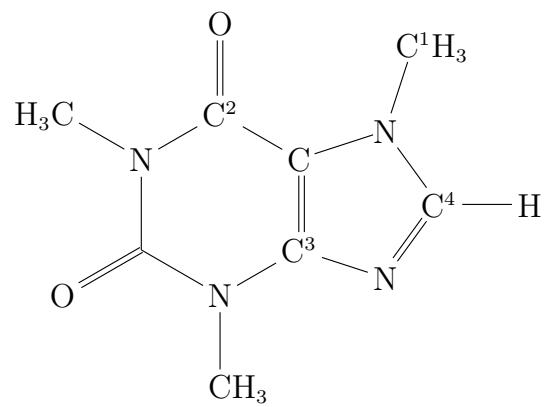
¿Qué nombre recibe el compuesto que se forma al hacer reaccionar benceno, , con bromo, , en presencia de bromuro de hierro(III), ?
Escriba la fórmula estructural desarrollada de dicho compuesto.
¿Qué tipo de reacción ha tenido lugar?
Ejercicio 8
8
2 puntosSe muestra, a continuación, la fórmula estructural desarrollada del metanol. Justifique, utilizando la teoría de la repulsión de los pares de electrones de la capa de valencia (TRPECV), los valores aproximados que toman los ángulos y .
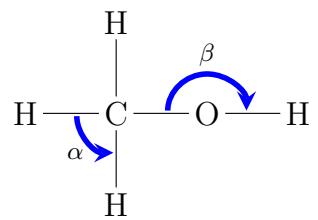
Calcule la incertidumbre asociada a la posición de un electrón si la incertidumbre asociada a su velocidad es .
Datos
Escriba la fórmula estructural desarrollada de los siguientes compuestos: 1-etil-4-metilciclohexano, 3-etil-5-metilheptano y 6-metilhept-2-en-4-ol.
Ejercicio 9
9
2 puntosEn un vaso de precipitados, a presión atmosférica y temperatura ambiente, se lleva a cabo la siguiente reacción: El anión y el catión son incoloros. Sin embargo, el anión presenta un color violeta intenso. Al mezclar los reactivos, el color violeta persiste durante, aproximadamente, un par de minutos. Transcurrido ese tiempo, el color de la disolución empieza a perder intensidad y lo hace cada vez más deprisa, hasta que, finalmente, desaparece por completo. Si la reacción se repite, a presión atmosférica, pero a , el color violeta inicial comienza a atenuarse al poco de mezclar los reactivos y la reacción termina muy rápidamente. Sabiendo que el catión es un catalizador de la reacción, utilice la ecuación de Arrhenius para explicar los fenómenos observados.
Escriba la fórmula estructural desarrollada del monómero que constituye el poli(cloruro de vinilo).
¿Qué tipo de polimeración se sigue en la formación del poli(cloruro de vinilo)?
Ejercicio 10
10
2 puntosEn un matraz Erlenmeyer se colocan de una disolución acuosa de ácido acético, , de concentración desconocida. Utilizando una bureta, se añade al Erlenmeyer, lentamente, una disolución acuosa de hidróxido de sodio, , , a la vez que se va registrando el pH de la misma. Los resultados se muestran en la figura. Calcule la concentración de la disolución acuosa de ácido acético.
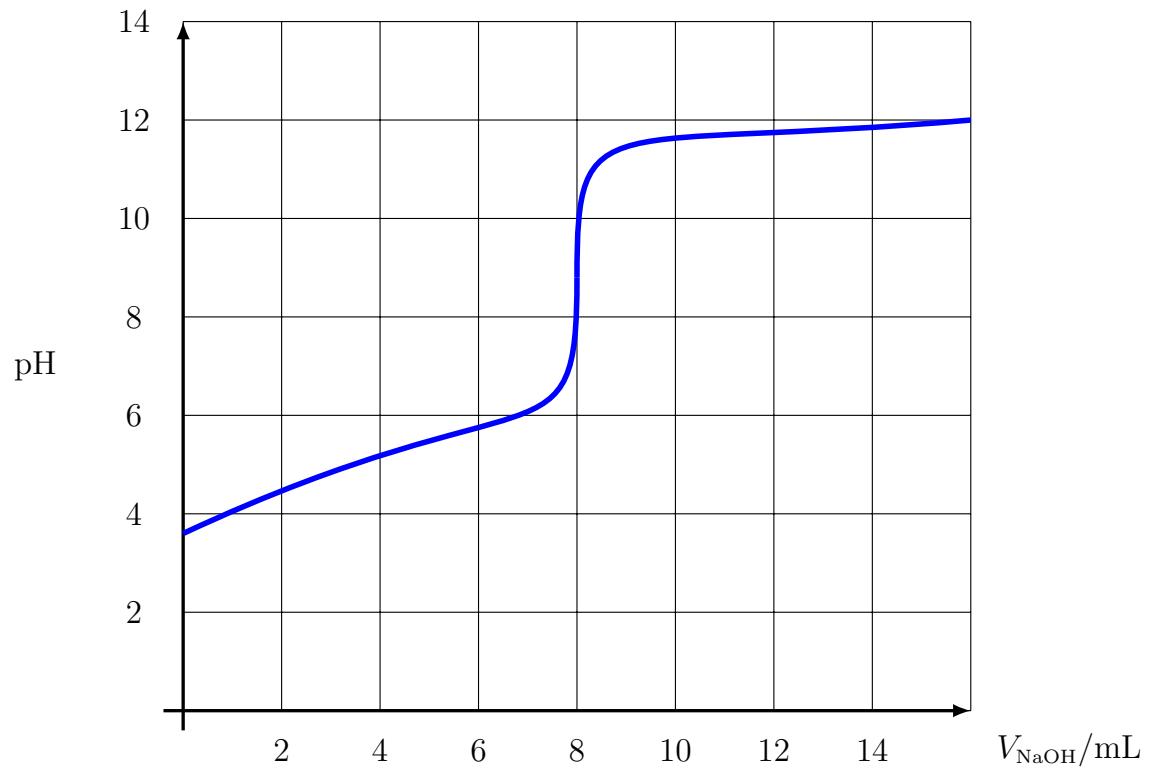
Se muestra, a continuación, la fórmula estructural desarrollada de la vitamina C.
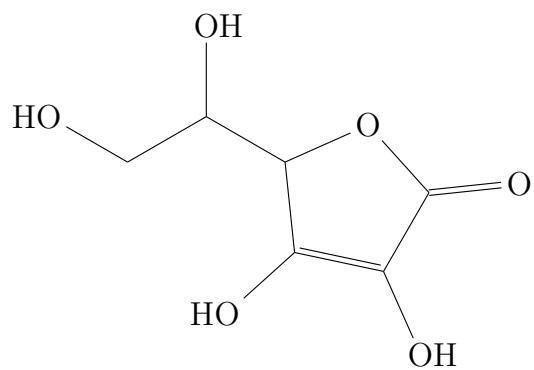
Escriba su fórmula molecular.
Copie en el pliego en blanco la fórmula del compuesto y señale todos los átomos de carbono asimétricos.
