Calcule el orden de la reacción respecto al .
QuímicaAsturiasPAU 2023Ordinaria
Química · Asturias 2023
10 ejercicios90 min de duración
Ejercicio 1
1
2 puntosEn la tabla se muestran los números atómicos, , las configuraciones electrónicas y el número de electrones desapareados de dos iones (1 y 2). Suponga que los dos electrones desapareados del ion 1 tienen espines paralelos. Indique, para cada ion, razonadamente, su carga eléctrica y si se encuentra en su estado fundamental o en uno excitado.
| Configuración electrónica | N.° de electrones desapareados | ||
| 1 | 7 | 2 | |
| 2 | 16 | 1 |
Ejercicio 2
2
2 puntosEl radio atómico del fósforo (, ) es y su primera energía de ionización es . Estime, razonadamente, para los átomos de nitrógeno (, ) y cloro (, ), si los valores de esas dos propiedades son mayores, menores o iguales que los del átomo de fósforo.
Ejercicio 3
3
2 puntosLa constante de equilibrio para la reacción a una temperatura , es (cuando las concentraciones se expresan en ). En un recipiente de volumen , a una temperatura , se introduce en exceso. Calcule las concentraciones de y cuando se alcanza el estado de equilibrio.
Ejercicio 4
4
2 puntosSe ha medido la velocidad inicial de la reacción siempre a la misma temperatura, pero en cuatro condiciones iniciales diferentes.
| Exp. | [CH3COCH3(aq)]0/(mol L-1) | [Br2(aq)]0/(mol L-1) | [H+(aq)]0/(mol L-1) | v0/(mol L-1s-1) |
| 1 | 1,00 | 1,00 | 1,00 | 4,0·10-3 |
| 2 | 2,00 | 1,00 | 1,00 | 8,0·10-3 |
| 3 | 2,00 | 2,00 | 1,00 | 8,0·10-3 |
| 4 | 1,00 | 1,00 | 2,00 | 8,0·10-3 |
Calcule el orden de la reacción respecto al .
Calcule el orden de la reacción respecto al .
Calcule el orden total de la reacción.
Calcule la constante cinética.
Escriba la ley de velocidad.
Ejercicio 5
5
2 puntosCalcule, a , el pH de una disolución acuosa de ().
Ejercicio 6
6
2 puntosCalcule la energía de Gibbs estándar de reacción, , a , del siguiente proceso:
| 2,076 | |
| 1,229 |
Ejercicio 7
7
2 puntosEscriba el nombre del material de laboratorio utilizado en la realización de una volumetría ácido-base.
La constante de equilibrio del proceso es 54 a una temperatura determinada. Calcule el valor de del proceso a la misma temperatura.
Ejercicio 8
8
2 puntosEscriba el procedimiento experimental seguido en la realización de una volumetría ácido-base.
En un vaso de precipitados, a presión atmosférica y temperatura ambiente, se establece el siguiente equilibrio químico: El complejo es incoloro, lo mismo que el anión . El complejo , por el contrario, presenta un color rojo intenso. Si, una vez establecido el equilibrio químico, se calienta el vaso de precipitados, se observa que la intensidad del color rojo de la disolución disminuye. Explique, a partir de esta observación, si la reacción es endotérmica o exotérmica.
Ejercicio 9
9
2 puntos¿Cuántos enlaces y hay en la molécula ?
Escriba las fórmulas moleculares correspondientes a las siguientes fórmulas estructurales semidesarrolladas e identifique cada compuesto como un alcano, un alqueno o un hidrocarburo aromático.
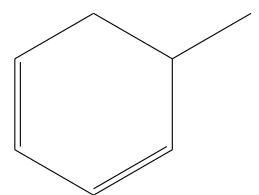
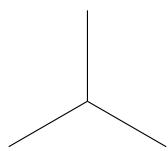
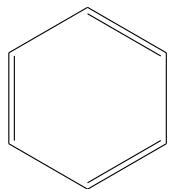
Ejercicio 10
10
2 puntosUtilice los datos de la tabla para, razonadamente, ordenar, de menor a mayor, los gases nobles atendiendo a su punto de ebullición.
| He | Ne | Ar | Kr | |
| 2 | 10 | 18 | 36 |
¿Qué nombre recibe el compuesto que se forma al hacer reaccionar ácido acético con etanol en presencia de ácido sulfúrico, , y aplicando calor?
Escriba la fórmula estructural semidesarrollada de dicho compuesto.
¿Qué tipo de reacción ha tenido lugar?
